US Pharm. 2014;39(11):38-41.
ABSTRACT: O síndrome de privação de álcool (AWS) pode ocorrer quando um indivíduo pára ou mesmo reduz significativamente o consumo de álcool após um período prolongado de utilização. Sintomas ligeiros podem ocorrer dentro de horas após a última bebida e, se não forem tratados, podem evoluir para sintomas mais graves, com risco de vida. Dependendo da gravidade dos sintomas de abstinência, os pacientes podem ser tratados em regime de internamento ou ambulatório. A farmacoterapia é muitas vezes necessária para tratar pacientes com AWS para gerir os sintomas de abstinência, prevenir a progressão para complicações graves, e fazer a ponte entre estes pacientes e o tratamento para manter a recuperação a longo prazo. Embora uma variedade de drogas tenha alguma utilidade no tratamento deste transtorno, as benzodiazepinas continuam a ser os agentes de escolha.
O Manual de Diagnóstico e Estatística dos Transtornos Mentais, Quinta Edição (DSM-5) combina o abuso e a dependência do álcool no recém-designado transtorno do uso de álcool (AUD).1 De acordo com o National Institute on Alcohol Abuse and Alcoholism (NIAAA), os transtornos do uso de álcool são condições médicas que ocorrem em pacientes que sofrem angústia ou danos relacionados com o seu consumo de bebidas alcoólicas. Aproximadamente metade dos pacientes com dependência alcoólica desenvolverão sintomas clinicamente relevantes de abstinência. Consequências mais graves da abstinência do álcool, especialmente convulsões ou delirium tremens (DTs), ocorrem em <5% dos pacientes dependentes de álcool.2
O Inquérito Nacional sobre o Uso de Drogas e Saúde de 2012 relatou que 7,2% dos adultos (17 milhões de pessoas com ³18 anos de idade) tinham um AUD.3,4 Dentro deste grupo, 24,6% reportaram ter-se envolvido em consumo excessivo no mês passado, enquanto 7,1% reportaram consumo excessivo durante este tempo.5 O consumo excessivo é definido como “um padrão de consumo que leva os níveis de concentração de álcool no sangue a 0,08 g/dL”; ou seja, normalmente 5 bebidas para homens e 4 bebidas para mulheres em 2 horas.6 Beber pesado é definido como “beber 5 ou mais bebidas na mesma ocasião em cada um de 5 ou mais dias nos últimos 30 dias”.6 Talvez mais significativamente, quase 900.000 adolescentes (com idades entre 12-17 anos) tiveram um AUD.7
PATIENTES CRIANÇADOS PARA O MISUSO DO ÁLCOOL
O USPSTF (U.S. Preventive Services Task Force) recomenda o rastreio de todos os pacientes adultos para o abuso do álcool.8 Três ferramentas primárias devem ser consideradas: o Teste de Identificação de Distúrbios do Uso de Álcool (AUDIT), a abreviatura AUDIT-Consumption (AUDIT-C), e o rastreio de uma única pergunta. Por exemplo, o NIAAA sugere perguntar aos pacientes: “Quantas vezes no último ano bebeu 5 (para homens) ou 4 (para mulheres e todos os adultos com mais de 65 anos) ou mais bebidas num dia? “8 Outra ferramenta de rastreio comummente utilizada é a pergunta-naire Cut-Down, Annoyed, Guilty, and Eye-Opener (CAGE).9 Todos estes são testes validados que os clínicos podem utilizar em ambulatório para avaliar os pacientes quanto ao abuso do álcool.
Aprovar os pacientes quanto ao abuso do álcool pode abrir os olhos e ser benéfico para alguns pacientes na mudança dos seus hábitos de consumo antes de surgirem quaisquer complicações como a síndrome de privação de álcool (AWS). Avaliar os pacientes desta forma permite que os clínicos forneçam aconselhamento àqueles que se envolvem em padrões de consumo de risco.
SÍNDROME DO ÁLCOOL COM SÍNDROME
Indivíduos que tenham bebido muito durante um período de tempo prolongado e reduzam significativamente o seu consumo de álcool ou parem abruptamente podem desenvolver AWS.10 Esta síndroma pode ser diagnosticada se um paciente experimentar quaisquer dois dos seguintes sintomas após a redução ou descontinuação do consumo de álcool: hiperactividade autonómica (por exemplo sudação ou ritmo cardíaco >100 bpm); aumento do tremor das mãos; insónia; náuseas ou vómitos; alucinações ou ilusões visuais, tácteis ou auditivas transitórias; agitação psicomotora; ansiedade; ou convulsões tónico-clónicas.1,11
AWS consiste em três ou quatro fases (dependendo da fonte) de gravidade, que se baseiam nos sintomas que um paciente está a experimentar.10,12 As fases 1 e 2 de retirada caracterizam-se por sintomas mais suaves, que podem fazer com que um paciente que ainda não esteja em tratamento comece novamente a consumir álcool.5 A fase 3 caracteriza-se por sintomas semelhantes com um aumento da gravidade e a adição de convulsões.13 A fase 4 inclui os sintomas anteriores em conjunto com os DTs. Os sintomas primários dos TD consistem em diaforese, febre, pesadelos, agitação, confusão global, desorientação, alucinações visuais e auditivas, e complicações cardiovasculares e metabólicas.10,13 A taxa de mortalidade dos pacientes que sofrem de TD tem sido relatada como sendo de 1% a 15%.12,14
Patofisiologia
Dois neurotransmissores no cérebro são afectados pelo consumo crónico de álcool e desempenham um papel importante no AWS. O ácido gama-aminobutírico (GABA) é o neurotransmissor inibitório primário e o glutamato é o neurotransmissor excitatório primário. Juntos, estes neurotransmissores mantêm o equilíbrio neuroquímico no cérebro. A presença de álcool inibe a função do receptor de N-metil-d-aspartato (NMDA), conduzindo aos efeitos sedativos e ansiolíticos do álcool, bem como à perda de memória e à geração de crises potencialmente fatais.13,15 Durante a retirada, os níveis de GABA diminuem abaixo da capacidade normal, o que acaba por levar à hiperactividade do sistema nervoso. Ao mesmo tempo, o glutamato é activado, o que por sua vez aumenta a função dos receptores NMDA.12,13
Foi proposto um processo conhecido como kindling para explicar a diminuição no tempo de início e o aumento da gravidade dos sintomas em pacientes que foram submetidos a repetidos episódios de abstinência. Isto está relacionado com as frequentes alterações nos receptores GABA e NMDA, como descrito acima.11,12
Assessment of Alcohol Withdrawal
A escala do Clinical Institute for Withdrawal Assessment for Alcohol-revised (CIWA-Ar) é um instrumento validado para avaliar a gravidade do AWS.16 Esta ferramenta é utilizada para monitorizar sinais e sintomas de abstinência e avaliar a necessidade de medicação. A escala CIWA-Ar lista 10 sinais e sintomas de abstinência que podem ser quantificados a fim de avaliar a gravidade da síndrome. Estes incluem náuseas e vómitos, perturbações auditivas, dores de cabeça, perturbações tácteis, suores paroxísticos, agitação, tremores, distúrbios visuais, orientação e turvação do sensorium, e ansiedade. Nove dos 10 sinais e sintomas podem ser classificados em gravidade de 0 a 7 e um de 0 a 4. A pontuação máxima possível é 67. Uma pontuação £8 indica retirada ausente ou muito ligeira; 9 a 14 indica retirada ligeira; 15 a 20 indica retirada moderada; e uma pontuação de >20 indica retirada grave.10
Configuração de tratamento
Patientes com AWS podem ser tratados em regime de internamento ou ambulatório, dependendo da gravidade da retirada. Para pacientes com AWS suave ou moderado, um ambiente de ambulatório em comparação com o hospital pode ser relativamente seguro e eficaz, ter custos mais baixos e ser aceitável devido ao impacto reduzido na vida pessoal do paciente.10,17 As contra-indicações ao tratamento ambulatório incluem resultados laboratoriais anormais, ausência de rede de apoio, doença aguda, alto risco de TD, historial de convulsões de abstinência, condições médicas crónicas mal controladas, condições psiquiátricas graves, incluindo ideação suicida, sintomas graves de abstinência de álcool, ou abuso de outras substâncias.17-19
TREATAMENTO
Os objectivos do tratamento AWS são gerir os sinais e sintomas da abstinência de álcool, prevenir a progressão para complicações médicas graves, e fazer a ponte entre os pacientes para o tratamento para manter a recuperação a longo prazo.10 Os pacientes com sintomas muito ligeiros podem necessitar apenas de cuidados de apoio, enquanto os pacientes com sintomas moderados a graves podem justificar uma intervenção farmacológica.19
Apoio Nutricional
Devem ser prestados apoios nutricionais, tal como tolerados, aos pacientes com AWS. Como parte desse apoio, a tiamina e o ácido fólico devem ser administrados rotineiramente. Recomenda-se a suplementação com ácido fólico de 1 mg diários. A suplementação de tiamina impede o desenvolvimento da encefalopatia de Wernicke, devendo ser administrada uma dose de 100 mg diários a todos os pacientes.10 Nos casos em que se suspeite da encefalopatia de Wernicke, recomenda-se a administração de vitaminas de alta potência com 500 mg de tiamina por via intravenosa três vezes por dia durante 3 dias.20
A suplementação de magnésio também foi recomendada uma vez que os níveis de magnésio no soro demonstraram ser baixos durante a privação de álcool. No entanto, os níveis de magnésio parecem voltar ao normal espontaneamente à medida que a AWS se aproxima da conclusão. Além disso, a suplementação de magnésio não demonstrou qualquer benefício no tratamento de AWS.19
Drug Therapy
Benzodiazepines: Os benzodiazepínicos são preferidos e são considerados tratamento de primeira linha em pacientes com AWS.15,17 Estes agentes reduzem os sintomas de abstinência incluindo convulsões e ajudam a prevenir a progressão dos sintomas.10,15 Os benzodiazepínicos de acção longa e intermédia são utilizados para tratar AWS. Os agentes de longa acção incluem clordiazepóxido (14- a 100-h de meia-vida dos metabolitos activos) e diazepam (30-100 h). Os agentes de acção intermédia são lorazepam (12-h meia-vida), oxazepam (5-15 h), e alprazolam (6-26 h).21 Não há fortes evidências de que qualquer medicação seja superior no tratamento AWS. Contudo, acredita-se que os benzodiazepínicos de acção prolongada podem proporcionar um efeito de retirada mais suave do que os intermediários.10,17 Em doentes com função hepática reduzida, incluindo os idosos, os agentes de acção intermédia podem ser mais seguros porque não possuem metabolitos activos. Além disso, estes agentes têm um potencial reduzido de sedação e depressão respiratória.13,19 As doses devem ser individualizadas para controlar os sintomas do doente e, em caso de abstinência resistente do álcool, podem ser necessárias doses muito grandes, embora a depressão respiratória possa ser uma complicação.13
Existem dois regimes distintos amplamente utilizados para administrar benzodiazepinas para AWS, um programa de dose fixa e um programa de dose desencadeada por sintomas (TABELA 1).10,13,22 O programa de dose fixa utiliza doses específicas a intervalos regulares, embora permita a administração de doses adicionais conforme necessário para controlar ainda mais os sintomas.22 O esquema de dose fixa utiliza benzodiazepinas a serem administradas apenas quando o paciente tem sintomas significativos representados por uma pontuação CIWA-Ar >9. Estudos demonstraram que o regime desencadeado pelos sintomas pode reduzir a utilização de medicamentos e encurtar a duração do tratamento.23,24
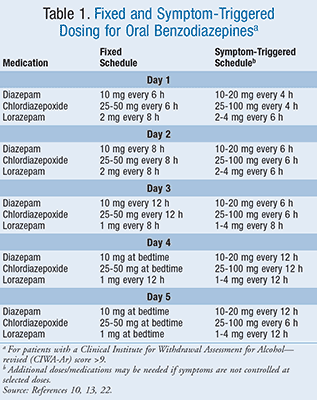
Num estudo realizado por Daeppen et al comparando a dosagem com frequência de sintomas com a dosagem com frequência fixa usando oxazepam para tratar a privação de álcool, a duração média da terapia e a dose total de oxazepam foi de 20 horas versus 62,7 horas e 37,5 mg versus 231,4 mg, respectivamente, sem qualquer diferença no conforto do doente.23 Este estudo analisou apenas o tratamento hospitalar.
p>Outros tratamentos com medicamentos: Os agentes neurolépticos como as fenotiazinas e o haloperidol podem reduzir a gravidade de alguns efeitos de retirada e podem ser benéficos em doentes com agitação descontrolada, embora haja poucos dados clínicos controlados que sustentem a sua utilização. Além disso, não são tão eficazes como as benzodiazepinas no bloqueio de delírios e convulsões.19
Existem alguns dados que sugerem que anticonvulsivos como carbamazepina, oxcarbazepina, e divalproex podem ser úteis no tratamento da dependência do álcool, reduzindo a ânsia de álcool e no tratamento AWS através do seu efeito anti-inflamatório.25-27 Ironicamente, estes agentes não impediram DTs ou apreensões.10 Num estudo, a gabapentina demonstrou ser eficaz no tratamento do AWS em comparação com o lorazepam. Além disso, pareceu reduzir a ânsia de abstinência de álcool.28 Tal como com os outros anticonvulsivos, são necessários ensaios mais controlados.
Barbituratos e propofol foram considerados eficazes em doentes com DTs refractários.29,30 Embora os barbitúricos sejam muito baratos, poucos estudos controlados foram realizados.19 Além disso, aumentam o risco de depressão respiratória quando combinados com o álcool.19 Há poucos dados disponíveis sobre o uso de propofol. Contudo, uma grande desvantagem da sua utilização é o seu elevado custo.30 Baclofen, um análogo estrutural de GABA utilizado como relaxante muscular esquelético, foi avaliado como tratamento para AWS. Os autores relataram que o baclofeno foi tão eficaz como o diazepam no tratamento AWS e mostra-se promissor como uma opção de tratamento.31
No entanto, são necessários mais ensaios clínicos controlados para medir a eficácia das não-benzodiazepinas no tratamento AWS e AUD. Enquanto não houver mais dados disponíveis para apoiar a utilização de outros agentes sobre as benzodiazepinas, estes continuarão a ser o tratamento de escolha. Os medicamentos utilizados no tratamento de AWS estão resumidos na TABELA 2.
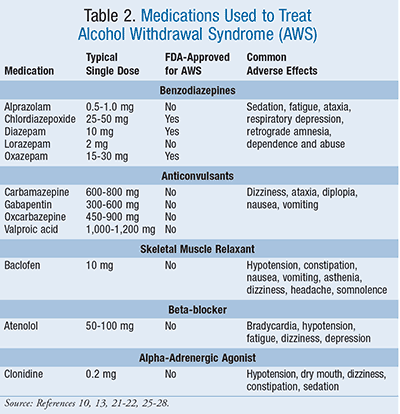
Terapia Ajuntiva: A terapia de ajustamento pode ter de ser adicionada à terapia benzodiazepínica, dependendo da apresentação do paciente. Os beta-bloqueadores e o agonista alfaadrenérgico clonidina podem ser adicionados para reduzir os sintomas adrenérgicos, tais como a redução da pressão arterial e do ritmo cardíaco e a redução dos tremores. No entanto, não impedem convulsões ou delírios.32 As opções de tratamento podem incluir qualquer um dos outros agentes discutidos anteriormente. A selecção do agente a utilizar é baseada nos sinais e sintomas específicos que estão a ser alvo. É importante notar que estes agentes adicionais não devem ser recomendados como monoterapia no tratamento AWS.10
MONITORING
A gravidade dos sintomas do paciente orienta a frequência da monitorização. Aqueles tratados como doentes internados podem ser inicialmente monitorizados e avaliados várias vezes por dia até que os sintomas melhorem. Uma vez estabilizado, o paciente pode ser avaliado diariamente até que os sintomas se resolvam e a dosagem da medicação seja reduzida. Após a conclusão do tratamento, os pacientes podem precisar de ser encaminhados para um programa de tratamento ambulatório a longo prazo, para um especialista em dependência, ou para um programa de tratamento ambulatório.5
PAPEL DO FARMACISTA
É importante que os farmacêuticos compreendam os AUDs, bem como os sinais, sintomas, e o tratamento do AWS. Uma vez que quase uma em cada 10 pessoas irá sofrer de dependência de alguma substância no decurso da sua vida, os farmacêuticos podem encontrar tais indivíduos diariamente. Uma vez que tal encontro ocorra, os farmacêuticos têm a oportunidade de aconselhar estes indivíduos sobre a doença e de fazer um encaminhamento para tratamento. No caso de tratamento ambulatório do AWS, os farmacêuticos podem aconselhar o paciente e/ou o prestador de cuidados sobre o uso adequado e os efeitos secundários dos medicamentos prescritos para tratar quer o AWS quer o próprio AUD, e podem estar disponíveis se e quando surgirem questões.
CONCLUSÃO
Por causa da gravidade e das complicações que podem surgir do AWS, é importante estar familiarizado com o tratamento adequado. O uso de benzodiazepinas é benéfico para diminuir a agitação, prevenir convulsões de retirada, e reduzir a progressão dos sintomas de retirada. Os farmacêuticos devem ser bem instruídos sobre os AUDs e o seu tratamento e sobre o tratamento do AWS para facilitar e optimizar o tratamento atempado e adequado do paciente, o que pode, em última análise, levar a salvar a vida de um paciente.
1. Associação Psiquiátrica Americana. Manual de Diagnóstico e Estatística das Doenças Mentais, Quinta Edição (DSM-5). Arlington, VA: American Psychiatric Publishing; 2013.
2. Schuckit M. Alcohol-use disorders. Lancet. 2009;373:492-501.
3. Substance Abuse and Mental Health Services Administration (SAMHSA). Inquérito Nacional sobre Uso de Drogas e Saúde (NSDUH) 2012. Tabela 5.8A. www.samhsa.gov/data/NSDUH/2012SummNatFindDetTables/DetTabs/NSDUH-DetTabsSect5peTabs1to56-2012.htm#Tab5.8A. Acedido a 7 de Agosto de 2014.
4. SAMHSA. 2012 NSDUH. Tabela 5.8B. www.samhsa.gov/data/NSDUH/2012SummNatFindDetTables/DetTabs/NSDUH-DetTabsSect5peTabs1to56-2012.htm#Tab5.8B. Acedido a 7 de Agosto de 2014.
5. SAMHSA. 2012 NSDUH. Tabela 2.26B. www.samhsa.gov/data/NSDUH/2012SummNatFindDetTables/DetTabs/NSDUH-DetTabsSect2peTabs43to84-2012.htm#Tab2.46B. Acedido a 7 de Agosto de 2014.
6. Factos e estatísticas sobre o álcool. Instituto Nacional sobre o Abuso do Álcool e o Alcoolismo. Julho de 2014. www.niaaa.nih.gov/alcohol-health/overview-alcohol-consumption/alcohol-facts-and-statistics. Acedido a 1 de Julho de 2014.
7. SAMHSA. 2012 NSDUH. Tabela 5.2A. www.samhsa.gov/data/NSDUH/2012SummNatFindDetTables/DetTabs/NSDUH-DetTabsSect5peTabs1to56-2012.htm#Tab5.2A. Acedido a 7 de Agosto de 2014.
8. U.S. Preventive Services Task Force. Rastreio e intervenções de aconselhamento comportamental nos cuidados primários para reduzir o abuso do álcool: declaração de recomendação. Maio de 2013. www.uspreventiveservicestaskforce.org/uspstf12/alcmisuse/alcmisusefinalrs.htm. Acedido a 1 de Fevereiro de 2014.
9. Testes de rastreio. Instituto Nacional sobre Abuso de Álcool e Alcoolismo. http://pubs.niaaa.nih.gov/publications/arh28-2/78-79.htm. Acedido a 8 de Agosto de 2014.
10. Muncie HL Jr, Yasinian Y, Oge’ L. Gestão ambulatorial da síndrome de abstinência de álcool. Am Fam Physician. 2013;88(9):589-595.
11. Lemon SJ, Winstead PS, Weant KA. Síndrome de privação de álcool. Adv Emerg Nurs J. 2010;32(1):20-27.
12. Perry EC. Gestão hospitalar da síndrome de privação aguda de álcool. Drogas do SNC. 2014;28:401-410.
13. Carlson RW, Kumar NN, Wong-McKinstry E, et al. Síndrome de privação de álcool. Clínica de Cuidados com os Critérios. 2012;28:549-585.
14. Ferguson JA, Suelzer CJ, Eckert GJ, et al. Factores de risco para o desenvolvimento de delirium tremens. J Gen Intern Med. 1996;11:410-414.
15. McKeon A, Frye MA, Delanty N. A síndrome de abstinência de álcool. J Neurol Neurosurg Psychiatry. 2008;79:854-862.
16. Sullivan JT, Sykora K, Schneiderman J, et al. Assessment of alcohol withdrawal: the revised Clinical Institute Withdrawal Assessment for Alcohol scale (CIWA-Ar). Br J Addict. 1989;84:1353-1357.
17. Myrick H, Anton RF. Tratamento da Retirada de Álcool. Mundo da Resina de Saúde Alcoólica. 1998;22(1):38-43.18. Kosten TR, O’Connor PG. Gestão da privação de drogas e álcool. N Engl J Med. 2003;348(18):1786-1795.
19. Mayo-Smith MF. Gestão farmacológica da retirada de álcool. Uma meta-análise e uma orientação de prática baseada em provas. Grupo de Trabalho sobre Gestão Farmacológica da Retirada de Álcool da Sociedade Americana de Medicina da Adicção. JAMA. 1997;278(2):144-151.
20. Thomson AD, Cook CC, Touquet CC, et al. O Royal College of Physicians report on alcohol: guidelines for managing Wernicke’s encephalopathy in the accident and emergency department. Álcool álcool Álcool. 2002;37:513-521.
21. Farmacologia Clínica . www.clinicalpharmacology.com. Acedido a 8 de Agosto de 2014.
22. Saitz R, Mayo-Smith MF, Roberts MS, et al. Tratamento individualizado para a privação de álcool. JAMA. 1994;272(7):519-523.
23. Daeppen JB, Gache P, Landry U, et al. Symptom-triggered vs fixed-schedule doses de benzodiazepina para a retirada de álcool: um ensaio de tratamento aleatório. Arch Intern Med. 2002;162(10):1117-1121.
24. Sachdeva A, Chandra M, Deshpande SN. Um estudo comparativo do regime de dose cónica fixa versus regime de lorazepam para desintoxicação alcoólica. Álcool Alcoólico Álcool. 2014;49(3):287-291.
25. Ait-Daoud N, Malcolm RJ Jr, Johnson BA. Uma visão geral dos medicamentos para o tratamento da abstinência e dependência do álcool com ênfase no uso de anticonvulsivos mais antigos e mais recentes. Comportamento de viciados. 2006;31(9):1628-1649.
26. Reoux JP, Saxon AJ, Malte CA, et al. Divalproex sodium in alcohol withdrawal: um ensaio clínico aleatório duplo-cego controlado por placebo. Alcohol Clin Exp Res. 2001;25(9):1324-1329.
27. Koethe D, Juelicher A, Nolden BM, et al. Oxcarbazepina-eficácia e tolerabilidade durante o tratamento da privação de álcool: um estudo-piloto multicêntrico duplo-cego, aleatorizado e controlado por placebo. Alcohol Clin Exp Res. 2007;31(7):1188-1194.
28. Myrick H, Malcolm R, Randall PK, et al. Um ensaio duplo-cego de gabapentina versus lorazepam no tratamento da privação de álcool. Alcohol Clin Exp Res. 2009;33(9):1582-1588.
29. Hack JB, Hoffmann RS, Nelson LS. Retirada de álcool resistente: será que uma necessidade de sedativos inesperadamente grande identifica estes pacientes precocemente? J Med Toxicol. 2006;2:55.
30. McCowan C, Marik P. Refractory delirium tremens tratados com propofol: uma série de casos. Crit Care Med. 2000;28:1781-1784.
31. Addolorato G, Leggio L, Abenavoli L, et al. Baclofen no tratamento da síndrome de abstinência de álcool: um estudo comparativo versus diazepam. Am J Med. 2006; 119(3):276.e13-276e18.
32. Robinson BJ, Robinson GM, Maling TJ, Johnson RH. A clonidina é útil no tratamento da privação de álcool? Alcohol Clin Exp Res. 1989;13:95-98.