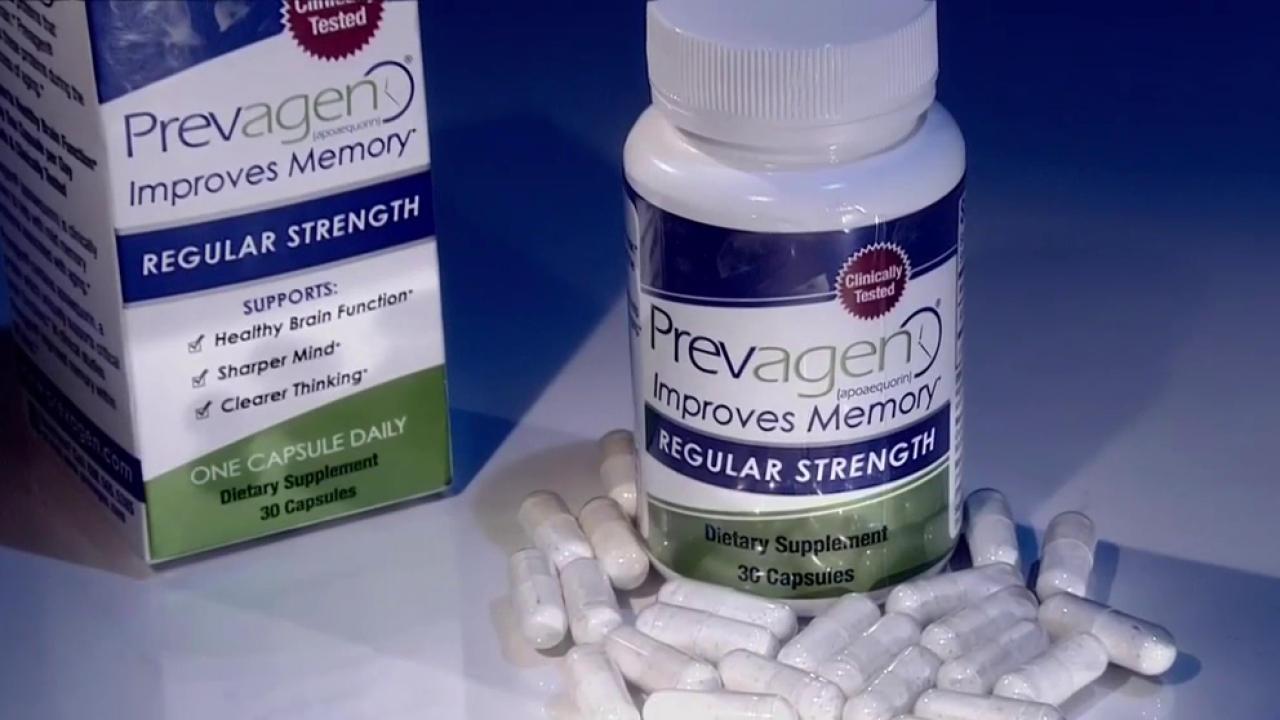
A Federal Trade Commission e o Procurador-Geral de Nova Iorque acusaram uma empresa com fraude na segunda-feira por vender um suplemento de memória baseado numa proteína de medusa brilhante.
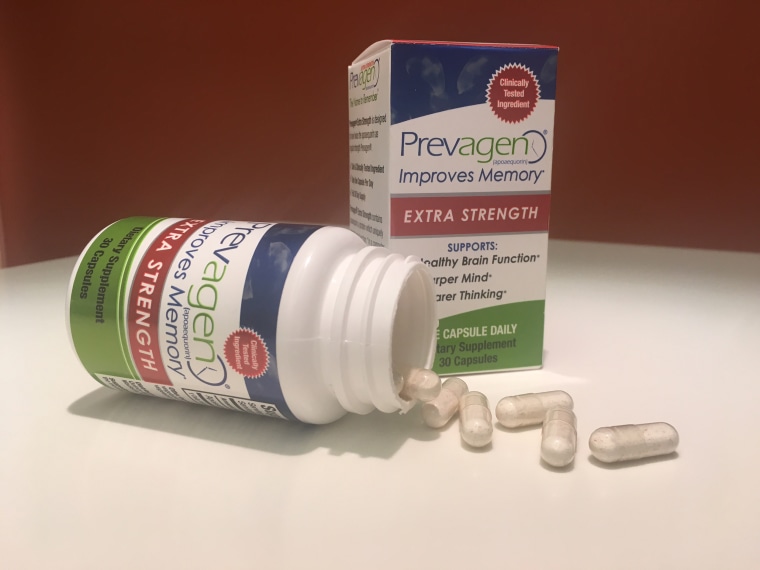
Os fabricantes de um produto chamado Prevagen estão a publicitá-lo falsamente como um impulsionador da memória, e alegando falsamente que o produto pode entrar no cérebro humano, as acusações reclamam.
Mas a empresa recuou muito, insistindo que o seu produto é seguro e chamando a FTC é uma agência federal “lame-duck” com cabeças que estão prestes a ser substituídas pela nova administração do presidente eleito Trump.
É a última batalha numa guerra em curso entre o governo federal e a Quincy Bioscience baseada no Wisconsin. Em 2012, a Food and Drug Administration apresentou uma carta de aviso à Quincy, dizendo que estava a fazer reivindicações médicas para um produto que não tinha passado pelo processo formal de aprovação de medicamentos.
Relacionado: Suplementos Enviar Milhares para ER
“A Comissão Federal de Comércio e o Procurador-Geral do Estado de Nova Iorque acusaram os comerciantes do suplemento dietético Prevagen de fazer alegações falsas e sem fundamento de que o produto melhora a memória, proporciona benefícios cognitivos, e está clinicamente demonstrado que funciona”, disse a FTC numa declaração.
“A extensa campanha publicitária nacional para Prevagen, incluindo spots televisivos em redes nacionais de radiodifusão e cabo como a CNN, Fox News, e NBC, apresentou gráficos que retratam uma melhoria rápida e dramática na memória dos utilizadores do produto.”
As cápsulas, que se vendem por qualquer valor entre $40 e $90 por uma garrafa, supostamente contêm uma proteína chamada apoaequorin, que é feita por algumas alforrecas que luminescem.
A empresa tentou, mas falhou, mostrar que pode ajudar as pessoas, diz a FTC.
“O Madison Memory Study não conseguiu mostrar uma melhoria estatisticamente significativa no grupo de tratamento”
“Os arguidos dependem principalmente de um estudo clínico humano duplo-cego, controlado por placebo, utilizando medidas objectivas de resultados da função cognitiva. Este estudo, denominado Estudo de Memória Madison, envolveu 218 sujeitos que tomaram 10 miligramas de Prevagen ou um placebo”, alega a carga.
“O Estudo de Memória Madison não conseguiu mostrar uma melhoria estatisticamente significativa no grupo de tratamento em relação ao grupo de placebo em qualquer uma das nove tarefas cognitivas computorizadas.”
A Associação Alzheimer não quis pesar sobre Prevagen em particular, mas a responsável científica da organização Maria Carrillo observou que não há nenhum produto por aí que tenha sido provado que ajude a memória.
“A Associação Alzheimer tem sérias preocupações sobre as pessoas que utilizam suplementos alimentares como alternativa ou para além das terapias prescritas por médicos, aprovadas pela FDA, numa tentativa de tratar ou prevenir a doença de Alzheimer ou outras demências”, disse ela.
“Antes de mais, a eficácia e segurança são desconhecidas. Além disso, a pureza do produto é desconhecida. Finalmente, os suplementos dietéticos podem ter sérias interacções com medicamentos prescritos”
Não obstante, a empresa disse que o estudo mostrou que o produto funciona.
“Os arguidos, contudo, não têm estudos que demonstrem que a apaequorin administrada oralmente pode atravessar a barreira cerebral do sangue humano e, portanto, não têm provas de que a apaequorin entra no cérebro humano”, de acordo com a acusação.
“Não há razão para um FTC com pouco pessoal e lame-duck para apressar esta queixa””
Na verdade não importa, porque o Prevagen é comercializado como suplemento.
A Lei de Saúde e Educação do Suplemento Alimentar (DSHEA), aprovada em 1994, isenta especificamente vitaminas e suplementos do escrutínio pré-comercialização da FDA, embora a agência possa advertir contra produtos considerados perigosos.
Relacionados: Vaccine Advocate Takes on Alternative Medicine Industry
E a FTC, assim como o Departamento de Justiça e funcionários do Estado, podem actuar contra práticas de marketing enganosas.
“Os profissionais de marketing de Prevagen aproveitam-se dos receios dos consumidores mais velhos que sofrem perdas de memória relacionadas com a idade”, disse Jessica Rich, directora do Gabinete de Defesa do Consumidor da FTC. “Mas uma coisa crítica que estes marqueteiros esqueceram é que as suas alegações precisam de ser apoiadas por provas científicas reais.
“O processo procura multar a Quincy e forçá-la a pagar aos consumidores que compraram os comprimidos.
“Antes de mais, a eficácia e a segurança são desconhecidas. Além disso, a pureza do produto é desconhecida””
No entanto, a empresa disse que iria combater as acusações.
“Discordamos veementemente destas alegações feitas por apenas dois comissários da FTC. Este caso é mais um exemplo do excesso de alcance governamental e dos reguladores que extinguem a inovação impondo novas regras arbitrárias a pequenas empresas como a nossa”, afirmou numa declaração.
“Não há razão para que uma FTC com falta de pessoal e de pessoal lamechas apresse esta queixa”.
Os membros do Congresso defendem frequentemente as empresas. A FDA queixou-se frequentemente de que DSHEA permite que os fabricantes de suplementos vendam produtos inúteis e muitas vezes prejudiciais aos consumidores confiantes, mas o Congresso não conseguiu rever a legislação.