 ¿Qué es mejor: un frasco de 100 dólares de Xalatan de marca o un frasco de 25 dólares de latanoprost genérico? Parece una pregunta fácil con una respuesta obvia, ¿verdad? Su paciente y el farmacéutico del paciente pueden pensar que sí, y no tienen reparos en elegir el genérico mucho más barato. Sin embargo, ¿debería usted ser tan consciente de los costes? Después de todo, si el genérico no funciona correctamente, incluso los 25 dólares son un desperdicio, y la visión del paciente puede estar en riesgo.
¿Qué es mejor: un frasco de 100 dólares de Xalatan de marca o un frasco de 25 dólares de latanoprost genérico? Parece una pregunta fácil con una respuesta obvia, ¿verdad? Su paciente y el farmacéutico del paciente pueden pensar que sí, y no tienen reparos en elegir el genérico mucho más barato. Sin embargo, ¿debería usted ser tan consciente de los costes? Después de todo, si el genérico no funciona correctamente, incluso los 25 dólares son un desperdicio, y la visión del paciente puede estar en riesgo.
A veces, efectivamente, se obtiene lo que se paga.
Por otro lado, los medicamentos genéricos funcionan lo suficientemente bien la mayoría de las veces y ofrecen un ahorro de costes muy real, no sólo para los pacientes individuales, sino también para el sistema de salud en su conjunto.
¿Cuándo es mejor prescribir el medicamento genérico o el de marca? Es una pregunta confusa. Pero con un poco más de información -que cubriremos en este artículo- es de esperar que tenga una mejor comprensión de cómo responderla para los pacientes individuales.
Basado en la bioequivalencia
Mientras que la compañía de marca inicial debe someterse a rigurosas pruebas de medicamentos y a largos ensayos clínicos cuando se presenta ante la Administración de Alimentos y Medicamentos (FDA), las compañías que producen medicamentos genéricos simplemente se someten a una forma abreviada del proceso de aprobación. La seguridad y la eficacia no tienen que ser probadas o establecidas con los genéricos porque se supone que ya se han realizado pruebas exhaustivas con el medicamento de marca. Las empresas sólo tienen que demostrar a la FDA que sus medicamentos son bioequivalentes a los de marca.1 En la actualidad, para demostrar la bioequivalencia, los científicos tienen que demostrar que el genérico se encuentra en un rango aceptable +/- de la concentración indicada. Normalmente, esto se consigue asegurando que la versión genérica libera su principio activo en el torrente sanguíneo a la misma velocidad y en la misma cantidad que el medicamento de marca.1
Aunque esto es relativamente fácil de medir con los medicamentos sistémicos, la bioequivalencia de los medicamentos oftálmicos no puede probarse de forma fiable de la misma manera. Además, es probable que las concentraciones en el torrente sanguíneo de un medicamento oftálmico aplicado directamente en el ojo no sean importantes para evaluar su eficacia. Por lo tanto, lo único que estipula la FDA para los medicamentos genéricos oftálmicos es que contengan la misma concentración del principio activo, la misma dosis y la misma vía de administración.2
Sin una verdadera prueba de bioequivalencia para los medicamentos oftálmicos, los profesionales del cuidado de los ojos deben asumir que funcionan igual de bien; sin embargo, todos sabemos que no siempre es así. La mayoría de los oftalmólogos probablemente recuerden la serie de pacientes de principios de la década de 2000 que experimentaron derrames corneales asociados al uso de la solución oftálmica de diclofenaco genérico (en contraposición al Voltaren de marca) después de una cirugía ocular. En un artículo, tres de cada cinco pacientes que experimentaron un derretimiento de la córnea tomaban diclofenaco genérico, y cuatro pacientes acabaron evolucionando hacia una perforación de la córnea que requirió un trasplante.3
Problemas potenciales con los genéricos
Los médicos y los analistas de la política sanitaria coinciden en gran medida en que los medicamentos genéricos pueden suponer un ahorro significativo en los costes de la atención sanitaria. Un estudio realizado en 2002 por el Instituto Schneider de Política Sanitaria de la Universidad de Brandeis indicaba que si se incrementaba el uso de genéricos por parte de los beneficiarios de Medicare, podría haber un ahorro teórico de miles de millones de dólares en atención sanitaria.4 Un informe de 2005 estimaba que por cada 1% de incremento en el uso de medicamentos genéricos, el gasto global en medicamentos recetados se reduciría entre 1.300 y 4.000 millones de dólares anuales.5
Por otro lado, es posible que las visitas de seguimiento al médico aumenten en número y/o frecuencia si la compañía de seguros o el paciente toman la decisión de cambiar a medicamentos genéricos. Esto podría anular efectivamente el ahorro en atención sanitaria.
Especialmente en el caso de los medicamentos para el glaucoma, algunos médicos pueden estar más inclinados a hacer volver a los pacientes antes para comprobar la eficacia y la tolerabilidad de la medicación genérica de lo que harían normalmente si no se hubiera producido el cambio. Debido al creciente número de fabricantes de genéricos y a la posible diferencia de eficacia entre ellos, un especialista en glaucoma ha llegado a recomendar el seguimiento de cada tipo de genérico haciendo que sus pacientes lleven los frascos a cada visita. De este modo, puede hacer un seguimiento de cada tipo de genérico y observar los patrones de eficacia y tolerabilidad.6
Aunque la FDA establece directrices definitivas para los medicamentos genéricos producidos en los Estados Unidos, las fábricas de fabricación en el extranjero pueden no ser supervisadas tan estrechamente. Aunque la solicitud de una empresa a la FDA debe incluir una descripción completa de las instalaciones que utiliza para la fabricación, las pruebas y el envasado, puede haber restricciones presupuestarias que impidan que todas las instalaciones en el extranjero sean inspeccionadas con el mismo calendario que las de Estados Unidos.7
También preocupa que los ingredientes de los medicamentos genéricos procedan de posibles fuentes con menos supervisión, como India y China. Por ejemplo, un estudio de 2005 descubrió que el 20% de las gotas oftálmicas genéricas de ciprofloxacina compradas en la India eran poco potentes, y algunas preparaciones del contenido del antibiótico eran lo suficientemente bajas como para afectar negativamente a los resultados del tratamiento.8
En el caso de los medicamentos genéricos, puede producirse un aumento de los síntomas de alergia de un mes a otro si hay una diferencia entre los fabricantes en los conservantes y/o ingredientes inactivos que utilizan. Si la farmacia recibe la medicación de diferentes empresas de un mes a otro, esto podría dar lugar a una mayor toxicidad de la superficie ocular, a una mala tolerabilidad y a que los pacientes vuelvan a la consulta de «ojos rojos».
Sólo tenemos que mirar hacia atrás para ver los problemas relacionados con Travatan (travoprost, Alcon) conservado con cloruro de benzalconio (BAK) para ver la posibilidad de que haya problemas con ciertos conservantes.9 Como se ha señalado anteriormente, a los medicamentos genéricos sólo se les exige que tengan la misma concentración del ingrediente activo, lo que significa que los ingredientes inactivos y los conservantes suelen ser diferentes. En consecuencia, un mayor número de visitas a la consulta para comprobar la eficacia y la tolerabilidad de un medicamento genérico podría, en teoría, hacer que aumentaran los costes de la atención oftalmológica y compensar el ahorro derivado del menor precio del medicamento.6
El creciente número de fabricantes de genéricos puede dar lugar a una apariencia incoherente de los frascos y a un aumento de la incertidumbre de los pacientes sobre su correcto cumplimiento. Los productores de medicamentos genéricos deben seguir las normas de fabricación y cumplir con las regulaciones de etiquetado, que prohíben que los frascos de medicamentos genéricos tengan un aspecto similar a sus homólogos de marca.10 Esto puede, en última instancia, causar confusión entre los pacientes si hay un color de tapa diferente, un color de etiqueta diferente o un tamaño de frasco que varía de un mes a otro. Un estudio reveló que el 36% de las personas dijeron que se sentirían molestas o preocupadas si el color o la apariencia del frasco de su medicamento cambiara de alguna manera.11
También se ha descubierto que algunos medicamentos genéricos tienen diferentes tamaños de cuentagotas, lo que puede variar el tamaño de las gotas, el número de dosis en el envase y, en última instancia, el coste del suministro de un mes.12 Además, se ha expresado preocupación por los plásticos utilizados en los frascos de los medicamentos y el control de calidad y lo que esto significa en términos de eficacia.6
Tenemos que reconocer la importancia de nuestro papel en la educación de los pacientes con respecto a estas posibles diferencias y asegurarnos de que nuestros pacientes se pongan en contacto con nosotros si tienen alguna pregunta sobre su tratamiento.
Estudios sobre los genéricos – Gotas para el glaucoma. En la actualidad, el medicamento oftálmico genérico que más titulares genera es latanoprost 0,005%, la versión comercial de Xalatan (Pfizer). En la actualidad, el «Libro Naranja», el texto de la FDA que contiene los «Medicamentos Aprobados con Equivalencia Terapéutica», enumera siete fabricantes aprobados de latanoprost genérico.13
– Gotas para el glaucoma. En la actualidad, el medicamento oftálmico genérico que más titulares genera es latanoprost 0,005%, la versión comercial de Xalatan (Pfizer). En la actualidad, el «Libro Naranja», el texto de la FDA que contiene los «Medicamentos Aprobados con Equivalencia Terapéutica», enumera siete fabricantes aprobados de latanoprost genérico.13
La eficacia de los medicamentos genéricos para el glaucoma es de especial interés en la comunidad oftalmológica. Aunque el genérico puede ser menos costoso y puede proporcionar un ahorro significativo, existe cierta preocupación de que los medicamentos genéricos para el glaucoma no tengan el mismo efecto que sus versiones comerciales, y el resultado podría ser la progresión de la enfermedad y la pérdida de visión.14
Sin embargo, un estudio reciente que comparó el latanoprost genérico con el Xalatan descubrió que ambos tratamientos demostraron una seguridad y tolerabilidad comparables entre los pacientes.15 Hay que tener en cuenta, no obstante, que el 99,6% de los pacientes del estudio eran blancos, por lo que estos resultados pueden no ser los mismos en afroamericanos, asiáticos e hispanos. Además, se podría argumentar que puede haber habido un sesgo del investigador porque Bausch + Lomb, el productor del genérico, llevó a cabo el estudio.
Previamente, sólo se había realizado otro estudio sobre una formulación genérica de latanoprost en 2007.16 El estudio consistió en 30 pacientes que fueron distribuidos aleatoriamente en dos grupos; recibieron Xalatan o un latanoprost genérico (Latoprost , producido en la India) durante las primeras 12 semanas, y luego cambiaron al otro medicamento durante las últimas 12 semanas. Los investigadores comprobaron que los pacientes que se pasaron de Latoprost a Xalatan experimentaron una mayor disminución de la PIO. En cambio, cuando los sujetos pasaron de Xalatan a Latoprost, la PIO aumentó más de 1 mm Hg de media. En general, el genérico, cuya fórmula tiene un pH más alto que el producto de marca, resultó ser menos eficaz para reducir la PIO.16
Al menos un estudio descubrió que el acetato de prednisolona genérico tiene partículas mucho más grandes, que se asientan fuera de la suspensión a un ritmo más rápido, se hunden en el fondo y requieren una mayor agitación por parte del paciente.
También se ha planteado la preocupación por la prescripción de la versión genérica de la solución gelificante de timolol. Los investigadores han demostrado que el tiempo de retención en la superficie ocular difiere entre los distintos vehículos de gel de liberación prolongada. En concreto, la goma gellan que se encuentra en Timoptic-XE (solución oftálmica de maleato de timolol, Merck) puede permitir que el medicamento de marca tenga un contacto más prolongado con la superficie, una mejor absorción y una actividad betabloqueante intraocular.17 En un estudio realizado en 2002, se demostró que la versión de marca de la solución gelificante de timolol basada en goma gellan disminuía la PIO mejor que su homóloga genérica basada en goma xantana.18 En consecuencia, algunas personas del ámbito médico han propuesto que deben evaluarse consideraciones, como el tamaño de las partículas y otras propiedades de una suspensión, para determinar la equivalencia genérica.19
– Gotas de esteroides. Varios estudios y casos de los últimos años también han ilustrado la necesidad de tener precaución y vigilancia al tratar la inflamación con esteroides oftálmicos. Allergan ha señalado en sus memorandos a los médicos que la suspensión microfina de su Pred Forte (acetato de prednisolona) es más uniforme, permanece más tiempo en el saco conjuntival y minimiza la irritación mecánica del ojo en comparación con el acetato de prednisolona genérico.20
Un estudio de 2007 analizó las diferencias en el tamaño de las partículas entre Pred Forte, EconoPred Plus y el acetato de prednisolona genérico al 1%.21 La hipótesis era que las partículas más grandes se asentarían fuera de la suspensión a un ritmo más rápido, se hundirían en el fondo y requerirían una mayor agitación por parte del paciente. Los resultados del estudio revelaron que la forma genérica de acetato de prednisolona tenía una mayor tendencia a la aglomeración de partículas, lo que posteriormente daba lugar a una concentración inconsistente de la dosis.21 Además, los autores escribieron que el mayor tamaño de las partículas podría obstruir la punta del frasco de medicación durante la instilación y alterar aún más la consistencia y la concentración de la dosis. Por el contrario, los tamaños de las partículas de Pred Forte eran más pequeños y uniformes, lo que permitía que permanecieran en suspensión durante más tiempo y proporcionaba una dosificación más precisa de la gota.21
Los optometristas deben tener en cuenta que los productos con ingredientes con poca suspensión pueden comprometer potencialmente el tratamiento de los ojos muy inflamados.
Perspectiva del paciente
– Coste y cumplimiento. En teoría, los medicamentos genéricos deberían mejorar el manejo y el cumplimiento del paciente porque se ha eliminado el obstáculo del coste. Con un análogo de prostaglandina más asequible ahora disponible, los pacientes que antes tomaban timolol genérico, dorzolamida genérica o los que habían rechazado el tratamiento pueden optar por tomar latanoprost genérico. Este tipo de cambio entre clases de medicamentos para el glaucoma también debería conducir a un cumplimiento significativamente mayor debido a la pauta de dosificación de la prostaglandina una vez al día.
– Complejo de inferioridad. Otro posible problema es que los pacientes pueden resistirse a tomar un medicamento genérico porque los perciben como inferiores a su homólogo de marca.22 Los genéricos se consideran a menudo medicamentos de segunda categoría debido a la percepción de un mal cumplimiento de las prácticas de fabricación estándar, a la falta de conocimiento de los pacientes sobre los genéricos y a la influencia de la empresa de marca.22,23 Según un estudio realizado en Nueva Zelanda, menos de la mitad de los participantes entrevistados percibían que los medicamentos genéricos eran seguros, eficaces y de igual calidad en comparación con su homólogo de marca.11
Además, el estudio neozelandés descubrió que los pacientes más jóvenes que tenían un mejor conocimiento y comprensión de las diferencias entre los fármacos eran más propensos que los que tenían un conocimiento deficiente de los mismos a decir que utilizarían un medicamento genérico tanto en enfermedades graves como leves.11 Tenemos que educar a nuestros pacientes para que puedan tomar una decisión informada sobre su tratamiento y estén dispuestos a probar un medicamento genérico si la situación es adecuada. Esto es especialmente cierto en los ancianos que pueden estar tomando múltiples medicamentos, así como en aquellos con un nivel socioeconómico bajo que podrían beneficiarse del ahorro.
– Las preferencias del paciente. A menudo tenemos que tener en cuenta la personalidad de nuestro paciente y su experiencia anterior al decidir entre medicamentos genéricos y de marca también. Una pregunta importante que debemos hacer a nuestros pacientes es si han tomado genéricos antes y cuál fue el resultado. Si el paciente tuvo una mala experiencia, puede estar predispuesto a los medicamentos de marca y dispuesto a pagar el precio más alto.
La gravedad de la enfermedad también puede influir en la disposición de un paciente a tomar un medicamento genérico. Según el mismo estudio realizado en Nueva Zelanda, los individuos encuestados estaban más dispuestos a cambiar a un genérico en el caso de una enfermedad leve que en el de una enfermedad grave (79% frente al 58,7%).11 En una enfermedad grave como el glaucoma, que tiene el potencial de provocar una pérdida de visión permanente, los pacientes pueden estar menos dispuestos a cambiar a un genérico.
¿Qué historia hay que creer?
La verdadera seguridad y eficacia de los medicamentos genéricos no puede asegurarse sin ensayos clínicos directos que comparen los medicamentos oftálmicos tópicos de marca con sus homólogos genéricos, pero actualmente los datos son limitados.19 Por ahora, esto es lo que hacemos:
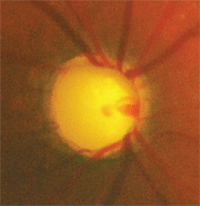
Un paciente con glaucoma avanzado o en fase terminal, que tiene un alto riesgo de progresión y pérdida de visión, probablemente debería seguir con la medicación de marca para mantener la PIO bajo buen control.
En pacientes con inflamación ocular secundaria a iritis, dada la investigación mencionada anteriormente, preferimos prescribir Pred Forte en lugar de un genérico siempre que sea posible.
De igual modo, debido a la falta de información sobre la eficacia de los medicamentos genéricos para el glaucoma, en los pacientes con glaucoma avanzado o en fase terminal que tienen un alto riesgo de progresión y pérdida de visión, consideramos firmemente seguir con la medicación de marca que tiene la PIO del paciente bajo buen control. No queremos arriesgarnos a perder el control de la enfermedad o causar toxicidad ocular al cambiar de marca a genérico.
Preparar una carta de valores para la aseguradora, en la que se indique que su paciente tiene «glaucoma avanzado o en fase final que amenaza la visión» y que ha estado estable con sus medicamentos actuales, será útil si se da esta situación. Otra opción es cambiar a los pacientes a un medicamento de marca para el que no haya un genérico disponible en ese momento (es decir, cambiar al paciente de Xalatan a una prostaglandina de otra marca), siempre que se consiga una eficacia similar.
En general, debemos educar a nuestros pacientes sobre el potencial de alergia y la poca eficacia de los medicamentos genéricos. Además, es posible que se necesiten más visitas a la consulta para evaluar el efecto reductor de la PIO entre los medicamentos genéricos y los de marca para el glaucoma, así como otros medicamentos oftálmicos.
Además, debemos decir a los pacientes que se pongan en contacto con nosotros si experimentan algún efecto adverso después de cambiar a un medicamento genérico. Siempre que la eficacia sea comparable y no se produzcan reacciones alérgicas, los genéricos proporcionan una opción de tratamiento alternativa y asequible que debería utilizarse y prescribirse a nuestros pacientes.
Como proveedores de atención oftalmológica, debemos recordar que al elegir entre medicamentos genéricos y de marca, hay dos lados de la historia.
Los doctores Chu y Hamp atienden a grandes poblaciones de pacientes con enfermedades avanzadas. Cada uno de ellos da conferencias sobre el glaucoma y otros temas clínicos. No tienen intereses financieros o de propiedad en ninguno de los medicamentos y/o compañías mencionados.
1. Cantor LB. Proceso de aprobación de medicamentos genéricos oftálmicos: implicaciones para la eficacia y la seguridad. J Glaucoma. 1997 Oct;6(5):344-9.
2. Fiscella RG. Sopesando la elección entre medicamentos genéricos y de marca. Insert to Cat Refr Surg Today. 2010 June. Disponible en: http://bmctoday.net/crstoday/2010/06/insert/article.asp?f=weighing-the-choice-between-generic-and-branded-drugs (consultado en enero de 2012).
3. Lin JC, Rapuano CJ, Laibson PR, et al. Corneal melting associated with use of topical nonsteroidal anti-inflammatory drugs after ocular surgery. Arch Ophthalmol. 2000 Aug;118(8):1129-32.
4. Administración de Alimentos y Medicamentos de los Estados Unidos. Greater Access to Generic Drugs: New FDA Initiatives to Improve the Drug Review Process and Reduce Legal Loopholes. Enero de 2006. Disponible en: www.fda.gov/drugs/resourcesforyou/consumers/ucm143545.htm (consultado en enero de 2012).
5. Audiencia del Subcomité de Salud del Comité de Energía y Comercio, Cámara de Representantes, 109º Congreso. Incrementar la utilización de medicamentos genéricos: Saving Money for Patients. 18 de mayo de 2005. Disponible en: www.gpo.gov/fdsys/pkg/CHRG-109hhrg21639/pdf/CHRG-109hhrg21639.pdf (consultado en enero de 2012).
6. Loewen NA, Realini T, Ruderman JM, Smit B. Xalatan goes generic: a landmark event in glaucoma. Glaucoma Today. Early Summer 2011:55-8.
7. U.S. Food and Drug Administration. La FDA garantiza la equivalencia de los medicamentos genéricos. Disponible en: www.fda.gov/Drugs/EmergencyPreparedness/BioterrorismandDrugPreparedness/ucm134444.htm (consultado en enero de 2012).
8. Weir RE, Zaidi FH, Charteris DG, et al. Variabilidad en el contenido de las gotas oftálmicas de ciprofloxacina genéricas de la India. Br J Ophthalmol. 2005 Sep;89(9):1094-6.
9. Baudouin C, Riancho L, Warnet JM, et al. Estudios in vitro de análogos de prostaglandinas antiglaucomatosas: travoprost con y sin cloruro de benzalconio y latanoprost conservado. Invest Ophthalmol Vis Sci. 2007 Sep;48(9):4123-8.
10. Gallardo MJ, Fiscella RG, Whitson JT. Medicamentos genéricos para el glaucoma. Glaucoma Today. 2006 Jan-Feb;4(1):32-5.
11. Babar ZU, Stewart J, Reddy S, et al. An evaluation of consumers’ knowledge, perceptions and attitudes regarding generic medicines in Auckland. Pharm World Sci. 2010 Aug;32(4):440-8.
12. Kirkner RM. Mitos y realidades del latanoprost genérico. Ophthalmic Office. 2011 Junio.
13. U.S. Food and Drug Administration. Orange Book: Medicamentos aprobados con evaluaciones de equivalencia terapéutica. Última actualización: 28 de octubre de 2011. Disponible en: www.accessdata.fda.gov/scripts/cder/ob/default.cfm (consultado en enero de 2012).
14. Bell NP, Ramos JL, Feldman RM. Seguridad, tolerabilidad y eficacia del tratamiento combinado fijo con dorzolamida hidrocolorida 2% y maleato de timolol 0,5% en glaucoma e hipertensión ocular. Clin Ophthalmol. 2010 Nov 22;4:1331-46.
15. Allaire C, Dietrich A, Allmeier H, et al. Latanoprost 0,005% formulación de prueba es tan eficaz como Xalatan en pacientes con hipertensión ocular y glaucoma primario de ángulo abierto. Eur J Ophthalmol. 2012 Jan;22(1):19-27.
16. Narayanaswamy A, Neog A, Baskaran M, et al. A randomized, crossover, open label pilot study to evaluate the efficacy and safety of Xalatan in comparison with generic latanoprost (Latoprost) in subjects with primary open angle glaucoma or ocular hypertension. Indian J Ophthalmol. 2007 Mar-Apr;55(2):127-31.
17. Meseguer G, Buri P, Plazonnet B, et al. Gamma scintigraphic comparison of eyedrops containing pilocarpine in healthy volunteers. J Ocul Pharmacol Ther. 1996 Winter;12(4):481-8.
18. Stewart WC, Sharpe ED, Stewart JA, Hott CE. The safety and efficacy of timolol 0.5% in xanthan gum versus timolol gel forming solution 0.5%. Curr Eye Res. 2002 May;24(5):387-91.
19. Fiscella RG, Gaynes BI, Jensen M. Equivalencia de productos oftálmicos genéricos y de marca. Am J Health Syst Pharm. 2001 Apr 1;58(7):616-7.
20. Allergan Medical Affairs. Información médica de las gotas oftálmicas Prednisolone Forte. Irvine, CA, comunicación del 19 de diciembre de 2011.
21. Roberts CW, Nelson PL. Análisis comparativo de las suspensiones de acetato de prednisolona. J Ocul Pharmacol Ther. 2007 Apr;23(2):182-7.
22. King DR, Kanavos P. Encouraging the use of generic medicines: implications for transition economies. Croat Med J. 2002 Aug;43(4):462-9.
23. Acta de la reunión del Comité Consultivo de Consumidores (CAC) de PHARMAC, 13 de julio de 2007; Wellington, Nueva Zelanda. Disponible en: www.pharmac.govt.nz/pdf/021007a.pdf (consultado en enero de 2012).
24. Investigación y fabricantes farmacéuticos de América. Comunicado de prensa: R&D La inversión de las empresas biofarmacéuticas estadounidenses alcanzó niveles récord en 2010. 15 de marzo de 2011; Washington, D.C. Disponible en: www.phrma.org/media/releases/rd-investment-us-biopharmaceutical-companies-reached-record-levels-2010 (consultado en enero de 2012).