12.6 L’échelle de pH
Objectifs d’apprentissage
- Définir le pH.
- Déterminer le pH des solutions acides et basiques.
Comme nous l’avons vu, les valeurs et peuvent être sensiblement différentes d’une solution aqueuse à l’autre. Les chimistes ont donc défini une nouvelle échelle qui indique succinctement les concentrations de l’un ou l’autre de ces deux ions.
pHTle logarithme négatif de la concentration en ions hydrogène. est une fonction logarithmique de :
pH = -log
pH est généralement (mais pas toujours) compris entre 0 et 14. Connaissant la dépendance du pH par rapport à , on peut résumer comme suit :
- Si le pH < 7, alors la solution est acide.
- Si le pH = 7, alors la solution est neutre.
- Si le pH > 7, alors la solution est basique.
C’est ce qu’on appelle l’échelle de pHLa gamme de valeurs de 0 à 14 qui décrit l’acidité ou la basicité d’une solution…. Vous pouvez utiliser le pH pour déterminer rapidement si une solution aqueuse donnée est acide, basique ou neutre.
Exemple 12
Etiqueter chaque solution comme acide, basique ou neutre en se basant uniquement sur le pH indiqué.
- Lait de magnésie, pH = 10.5
- eau pure, pH = 7
- vin, pH = 3,0
Solution
- Avec un pH supérieur à 7, le lait de magnésie est basique. (Le lait de magnésie est en grande partie Mg(OH)2.)
- L’eau pure, avec un pH de 7, est neutre.
- Avec un pH inférieur à 7, le vin est acide.
Testez-vous
Identifiez chaque substance comme acide, basique ou neutre en vous basant uniquement sur le pH indiqué.
- Sang humain, pH = 7,4
- Ammoniaque domestique, pH = 11.0
- les cerises, pH = 3,6
Réponses
- basique
- acide
Tableau 12.3 « Valeurs typiques du pH de diverses substances* » donne les valeurs typiques du pH de quelques substances courantes. Notez que plusieurs aliments figurent sur la liste, et que la plupart d’entre eux sont acides.
Tableau 12.3 Valeurs typiques du pH de diverses substances*
| Substance | pH |
|---|---|
| acide gastrique | 1.7 |
| Jus de citron | 2,2 |
| vinaigre | 2.9 |
| soda | 3,0 |
| vin | 3,5 |
| café noir | 5.0 |
| Lait | 6,9 | Eau pure | 7,0 | Sang | 7.4 |
| Eau de mer | 8,5 |
| Lait de magnésie | 10,5 | Solution ammoniacale | 12.5 |
| 1,0 M NaOH | 14,0 |
| *Les valeurs réelles peuvent varier en fonction des conditions. | |
Le pH est une échelle logarithmique. Une solution qui a un pH de 1,0 a 10 fois le comme une solution avec un pH de 2,0, qui à son tour a 10 fois le comme une solution avec un pH de 3,0 et ainsi de suite.
= 10-pH
Vous devez déterminer comment évaluer l’expression ci-dessus sur votre calculatrice. Demandez à votre instructeur si vous avez des questions. L’autre problème qui nous concerne ici est celui des chiffres significatifs. Parce que le ou les chiffres avant la virgule dans un logarithme se rapportent à la puissance sur 10, le nombre de chiffres après la virgule est ce qui détermine le nombre de chiffres significatifs dans la réponse finale :
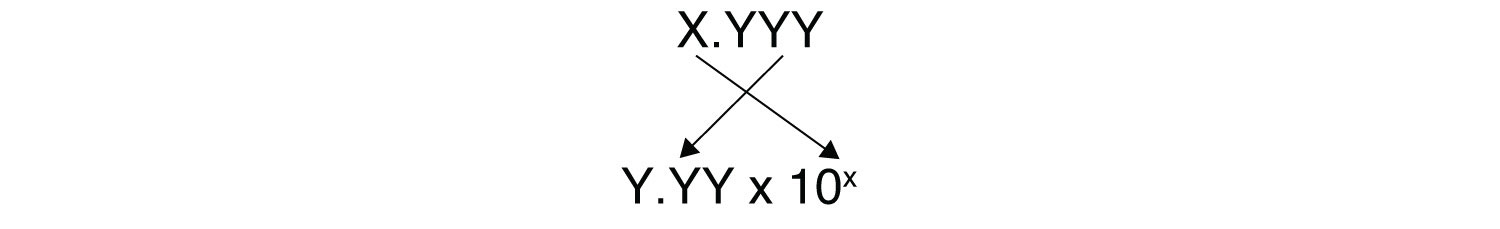
Il existe un moyen plus facile de relier et . Nous pouvons également définir pOHTle logarithme négatif de la concentration en ions hydroxyde. similaire au pH :
pOH = -log
(En fait, p « n’importe quoi » est défini comme le logarithme négatif de ce n’importe quoi.) Cela implique également que
= 10-pOH
Une relation simple et utile est que pour toute solution aqueuse,
pH + pOH = 14
Cette relation permet de déterminer facilement le pH à partir de pOH ou pOH à partir du pH, puis de calculer la concentration en ions qui en résulte.
Key Takeaways
- pH est une fonction logarithmique de .
- peut être calculé directement à partir du pH.
- pOH est lié au pH et peut être facilement calculé à partir du pH.
.