Formules moléculaires
Les formules moléculaires donnent le genre et le nombre d’atomes de chaque élément présent dans le composé moléculaire. Dans de nombreux cas, la formule moléculaire est la même que la formule empirique. La formule chimique sera toujours un certain multiple entier (\(n\)) de la formule empirique (c’est-à-dire des multiples entiers des indices de la formule empirique).
C’est pourquoi
Le multiple entier, n, peut également être obtenu en divisant la masse molaire, \(MM\), du composé par la masse de la formule empirique, \(EFM\) (la masse molaire représentée par la formule empirique).
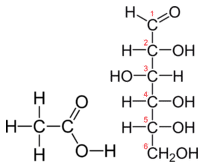
Le tableau \(\PageIndex{1}\) montre la comparaison entre la formule empirique et la formule moléculaire du méthane, de l’acide acétique et du glucose, et les différentes valeurs de n. La formule moléculaire du méthane est \(\ce{CH_4}\) et comme il ne contient qu’un seul atome de carbone, c’est également sa formule empirique. Parfois, cependant, la formule moléculaire est un simple multiple entier de la formule empirique. L’acide acétique est un acide organique qui est le principal composant du vinaigre. Sa formule moléculaire est : \(\ce{C_2H_4O_2}\). Le glucose est un sucre simple que les cellules utilisent comme principale source d’énergie. Sa formule moléculaire est \(\ce{C_6H_{12}O_6}\). Les structures de ces deux molécules sont illustrées sur la figure \(\PageIndex{2}\). Ce sont des composés très différents, mais ils ont tous deux la même formule empirique \(\ce{CH_2O}\).
| Nom du composé | Formule moléculaire | Formule empirique | n |
|---|---|---|---|
| Méthane | \(\ce{CH_4}\) | \(\ce{CH_4}\) | 1 |
| Acide acétique | \N(\ce{C_2H_4O_2}) | \N(\ce{CH_2O}\) | 2 |
| Glucose | \N(\ce{C_6H_{12}O_6}\) | \N(\ce{CH_2O}\) | 6 |
Les formules empiriques peuvent être déterminées à partir de la composition en pourcentage d’un composé, comme nous l’avons vu à la section 6.8. Afin de déterminer sa formule moléculaire, il est nécessaire de connaître la masse molaire du composé. Les chimistes utilisent un instrument appelé spectromètre de masse pour déterminer la masse molaire des composés. Pour passer de la formule empirique à la formule moléculaire, suivez les étapes suivantes :
- Calculer la masse molaire de la formule empirique (EFM).
- Diviser la masse molaire du composé par la masse molaire de la formule empirique. Le résultat doit être un nombre entier ou très proche d’un nombre entier.
- Multiplier tous les indices de la formule empirique par le nombre entier trouvé à l’étape 2. Le résultat est la formule moléculaire.
Exemple \(\PageIndex{1}\)
La formule empirique d’un composé de bore et d’hydrogène est \(\ce{BH_3}\). Sa masse molaire est \(27,7 \ : \text{g/mol}\). Déterminez la formule moléculaire de ce composé.
Solution
| Étapes de la résolution du problème | Déterminer la formule moléculaire de \(\ce{BH_3}\). |
|---|---|
| Identifiez les informations « données » et ce que le problème vous demande de « trouver ». » |
Donné : Formule empirique \(= \ce{BH_3}\) Masse molaire \(= 27,7 \ : \text{g/mol}\) Trouver : formule moléculaire \(= ?\) |
| Calculer la masse de la formule empirique (EFM). | \ |
| Diviser la masse molaire du composé par la masse de formule empirique. Le résultat doit être un nombre entier ou très proche d’un nombre entier. |
\ |
| Multipliez tous les indices de la formule empirique par le nombre entier trouvé à l’étape 2. Le résultat est la formule moléculaire. | |
| Écrivez la formule moléculaire. | La formule moléculaire du composé est \(\ce{B_2H_6}\). |
| Réfléchissez à votre résultat. | La masse molaire de la formule moléculaire correspond à la masse molaire du composé. |
Exercice \(\PageIndex{1}\)
La vitamine C (acide ascorbique) contient 40,92 % de C, 4,58 % de H et 54,50 % de O, en masse. La masse moléculaire déterminée expérimentalement est de 176 amu. Quelles sont les formules empirique et chimique de l’acide ascorbique ?
Réponse Formule empirique C3H4O3 Réponse Formule moléculaire C6H8O6
.