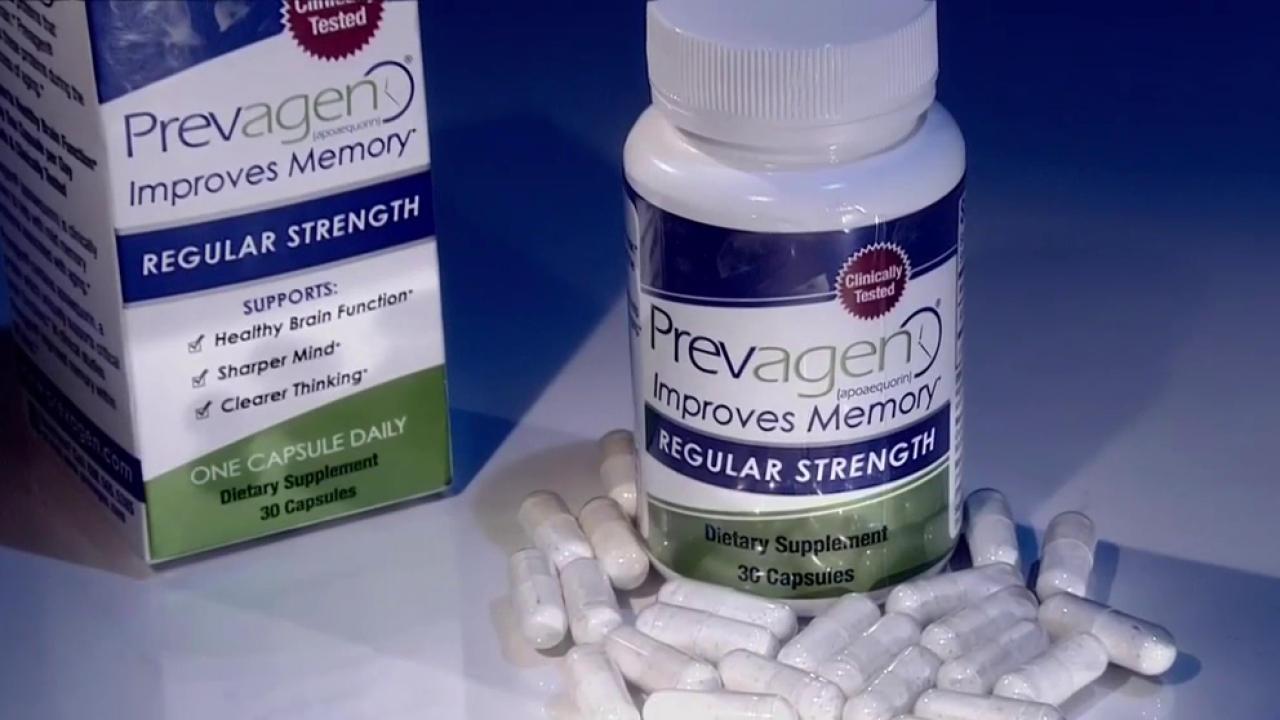
La Comisión Federal de Comercio y el fiscal general de Nueva York acusaron el lunes a una empresa de fraude por vender un suplemento para la memoria basado en una proteína de medusa brillante.
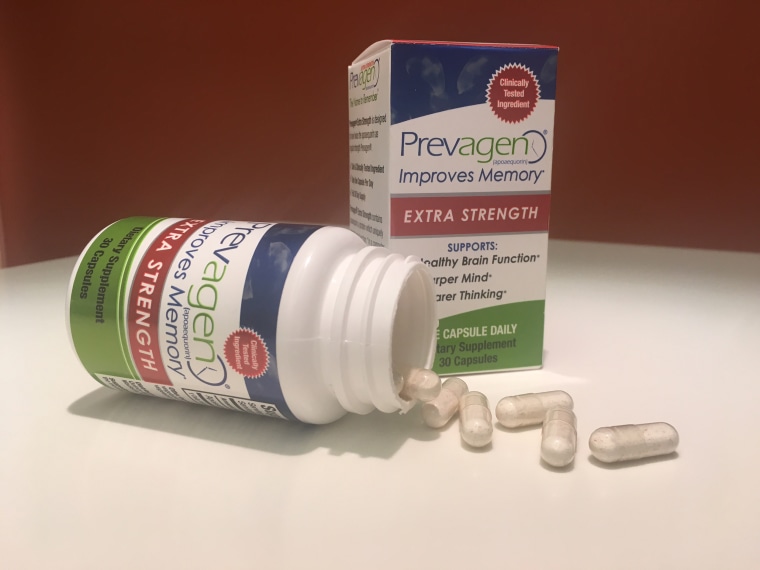
Los fabricantes de un producto llamado Prevagen lo anuncian falsamente como un potenciador de la memoria y afirman falsamente que el producto puede llegar al cerebro humano, según los cargos.
Pero la compañía se defendió con fuerza, insistiendo en que su producto es seguro y calificando a la FTC como una agencia federal «coja» con jefes que están a punto de ser reemplazados por la administración entrante del presidente electo Trump.
Es la última batalla en una guerra continua entre el gobierno federal y la empresa Quincy Bioscience, con sede en Wisconsin. En 2012, la Administración de Alimentos y Medicamentos presentó una carta de advertencia a Quincy, diciendo que estaba haciendo afirmaciones médicas para un producto que no había pasado por el proceso formal de aprobación de medicamentos.
Relacionado: Los suplementos envían a miles de personas a urgencias
«La Comisión Federal de Comercio y el Fiscal General del Estado de Nueva York han acusado a los comercializadores del suplemento dietético Prevagen de hacer afirmaciones falsas y sin fundamento de que el producto mejora la memoria, proporciona beneficios cognitivos y está clínicamente demostrado que funciona», dijo la FTC en un comunicado.
«La extensa campaña publicitaria nacional de Prevagen, que incluía anuncios de televisión en cadenas nacionales de radio y televisión por cable como CNN, Fox News y NBC, presentaba gráficos que mostraban una rápida y espectacular mejora de la memoria de los usuarios del producto.»
Las cápsulas, que se venden entre 40 y 90 dólares por un frasco, contienen supuestamente una proteína llamada apoaequorina, que es fabricada por algunas medusas que se iluminan.
La compañía intentó, pero no logró, demostrar que puede ayudar a las personas, dice la FTC.
«El estudio sobre la memoria de Madison no logró mostrar una mejora estadísticamente significativa en el grupo de tratamiento»
«Los demandados se basan principalmente en un estudio clínico en humanos, doble ciego y controlado con placebo, que utiliza medidas objetivas de resultados de la función cognitiva. En este estudio, denominado Estudio de la Memoria de Madison, participaron 218 sujetos que tomaron o bien 10 miligramos de Prevagen o bien un placebo», alega la acusación.
«El Estudio de la Memoria de Madison no pudo mostrar una mejora estadísticamente significativa en el grupo de tratamiento respecto al grupo de placebo en ninguna de las nueve tareas cognitivas informatizadas.»
La Asociación de Alzheimer no quiso opinar sobre Prevagen en particular, pero la responsable científica de la organización, María Carrillo, señaló que no existe ningún producto que haya demostrado ayudar a la memoria.
«La Asociación de Alzheimer tiene serias dudas sobre el uso de suplementos dietéticos como alternativa o complemento a las terapias prescritas por los médicos y aprobadas por la FDA en un intento de tratar o prevenir la enfermedad de Alzheimer u otras demencias», dijo.
«En primer lugar, se desconoce la eficacia y la seguridad. Además, se desconoce la pureza del producto. Por último, los suplementos dietéticos pueden tener graves interacciones con los medicamentos recetados.»
No obstante, la empresa dijo que el estudio sí demostró que el producto funciona.
«Los demandados, sin embargo, no tienen estudios que demuestren que la apoaequorina administrada por vía oral pueda atravesar la barrera hematoencefálica humana y, por tanto, no tienen pruebas de que la apoaequorina entre en el cerebro humano», según la acusación.
«No hay ninguna razón para que una FTC con poco personal y poco activa se apresure a presentar esta queja»
En realidad no importa, porque Prevagen se comercializa como un suplemento.
La Ley de Salud y Educación sobre Suplementos Dietéticos (DSHEA), aprobada en 1994, exime específicamente a las vitaminas y los suplementos del escrutinio previo a la comercialización de la FDA, aunque la agencia puede advertir sobre los productos que se consideren peligrosos.
Relacionado: El defensor de las vacunas se enfrenta a la industria de la medicina alternativa
Y la FTC, así como el Departamento de Justicia y las autoridades estatales, pueden actuar contra las prácticas de marketing engañosas.
«Los comercializadores de Prevagen se aprovecharon de los temores de los consumidores de edad avanzada que experimentan una pérdida de memoria relacionada con la edad», dijo Jessica Rich, directora de la Oficina de Protección al Consumidor de la FTC. «Pero algo fundamental que estos comercializadores olvidaron es que sus afirmaciones deben estar respaldadas por pruebas científicas reales».
La demanda pretende multar a Quincy y obligarla a devolver el dinero a los consumidores que compraron las píldoras.
«En primer lugar, se desconoce la eficacia y la seguridad. Además, se desconoce la pureza del producto»
Sin embargo, la compañía dijo que luchará contra las acusaciones.
«Estamos vehementemente en desacuerdo con estas acusaciones hechas por sólo dos comisionados de la FTC. Este caso es otro ejemplo de la extralimitación del gobierno y de los reguladores que extinguen la innovación imponiendo nuevas normas arbitrarias a pequeñas empresas como la nuestra», dijo en un comunicado.
«No hay razón para que una FTC con poco personal y poco productiva se apresure a presentar esta denuncia».
Los miembros del Congreso suelen defender a las empresas. La FDA se ha quejado con frecuencia de que la DSHEA permite a los fabricantes de suplementos vender productos inútiles y a menudo dañinos a consumidores confiados, pero el Congreso no ha revisado la legislación.