CONCEPTO DE LA BRECHA ANIÓN – SU DEFINICIÓN Y CÁLCULO
El plasma sanguíneo es una solución acuosa (agua) que contiene una plétora de especies químicas entre las que se encuentran algunas que tienen una carga eléctrica neta, resultado de la disociación de sales y ácidos en el medio acuoso. Las que tienen una carga positiva neta se denominan cationes y las que tienen una carga negativa neta se denominan aniones; en conjunto, estas especies con carga eléctrica se denominan iones.
La ley de la neutralidad electroquímica exige que, en común con todas las soluciones, el suero/plasma sanguíneo sea electroquímicamente neutro, de modo que la suma de la concentración de cationes sea siempre igual a la suma de la concentración de aniones .
Esta ley inmutable se refleja en la FIGURA 1, una representación gráfica de la concentración de los principales iones normalmente presentes en el plasma/suero. De ella se desprende que cuantitativamente el catión más significativo en el plasma es el sodio (Na+), y los aniones más significativos son el cloruro (Cl-) y el bicarbonato HCO3-.
La concentración de estos tres constituyentes plasmáticos (sodio, cloruro y bicarbonato) junto con el catión potasio (K+) se miden de forma rutinaria en el laboratorio clínico como parte del perfil bioquímico más frecuentemente solicitado, la urea y los electrolitos (U&E).
FIGURA 1: Anatomía iónica normal del suero
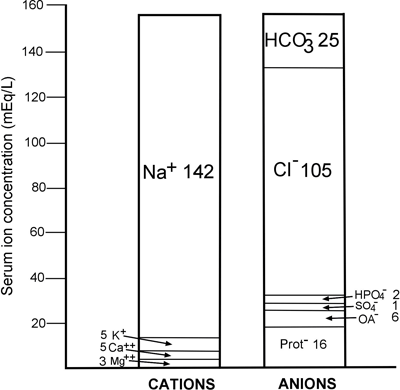
En la FIGURA 1 queda claro que la concentración del catión principal, el sodio (142 mmol/L), supera en 12 mmol/L las concentraciones combinadas de los dos aniones principales, el cloruro y el bicarbonato (130 mmol/L).
Esto es la brecha aniónica, que se define como la diferencia entre la concentración de sodio en plasma/suero y la suma de las concentraciones de cloruro y bicarbonato en plasma/suero :
| Anion gap (AG) (mmol/L) = – ( + ) Definición 1 | |
| Donde | = la concentración de sodio en plasma/suero (mmol/L) | = la concentración de cloruro en plasma/suero (mmol/L) |
| = la concentración de bicarbonato en plasma/suero (mmol/L) | |
Una alternativa, menos utilizada, permite incluir el catión potasio (K+):
Anion gap (AG) (mmol/L) = ( + ) – ( + ) Definición 2
Así, para un individuo con los siguientes valores de electrolitos plasmáticos:
| Sodio en plasma | 139 mmol/L |
| 4.0 mmol/L | |
| Cloruro de plasma | 103 mmol/L |
| Bicarbonato de plasma | 26 mmol/L |
| El gap aniónico es | O bien 139 – (103 + 26) = 10 mmol/L si se utiliza la definición 1 |
Desgraciadamente, sigue sin haber consenso sobre cuál de las dos definiciones se adopta, pero para una interpretación precisa de los resultados de los pacientes es obviamente importante saber cuál de las dos definiciones se ha utilizado. Para el resto de este artículo se utilizará la definición 1.
La brecha aniónica calculada es una construcción artificial que simplemente refleja el hecho de que la concentración de los cationes comúnmente medidos excede la concentración de los aniones comúnmente medidos.
La ley de neutralidad electroquímica exige que, en general, la brecha aniónica del suero, después de tener en cuenta la concentración combinada de todos los cationes y todos los aniones no medidos , debe ser cero:
La brecha aniónica (AG) = ( + ) – ( + + ) = 0
De esto se deduce que la brecha aniónica «calculada» refleja una desigualdad entre la concentración combinada de aniones no medidos y la concentración combinada de cationes no medidos , y subraya el importante punto de que la brecha aniónica calculada es tanto una función de la concentración de iones no medidos como de la concentración de los iones medidos (Na, Cl, HCO3) utilizados para hacer el cálculo. A partir de la ecuación anterior podemos afirmar que:
+ = + + y por reordenamiento
– ( + ) = –
y como la brecha aniónica (AG) = – ( + ) entonces
La brecha aniónica (AG) = –
Así la brecha aniónica también puede definirse como la diferencia entre los cationes no medidos y los aniones no medidos .
Gap aniónico – Intervalo de referencia
Hay inconsistencia en la literatura con respecto al intervalo de referencia del gap aniónico . Tradicionalmente, el intervalo de referencia ha sido ampliamente aceptado como 8-16 mmol/L si se excluye el potasio (definición 1) .
Esto se aproxima a 12-20 mmol/L si se incluye el potasio en el cálculo del AG. Los resultados de varios estudios sugieren un intervalo de referencia mucho más bajo, de 3-10 mmol/L. Este cambio en el intervalo de referencia se atribuye generalmente al cambio en la metodología utilizada para medir el sodio y el cloruro . La fotometría de llama fue una vez el único método para medir el sodio, y el cloruro se midió colorimétricamente.
Sin embargo, desde 1990 estas técnicas se han abandonado en gran medida en favor de la medición por electrodo selectivo de iones. Esta no puede ser toda la explicación porque sigue habiendo una diferencia significativa en la brecha aniónica calculada entre los analizadores modernos que utilizan todos electrodos selectivos de iones.
Por ejemplo, Roberts et al. compararon la brecha aniónica determinada mediante tres analizadores diferentes (todos ellos utilizan electrodos selectivos de iones) y concluyeron que el intervalo de referencia tradicional más alto de 8-16 mmol/L estaba cerca de ser apropiado para dos analizadores, pero era inapropiado para el tercero.
Para este analizador, el intervalo más bajo de 3-10 mmol/L era mucho más apropiado.
Paulson et al también mostraron que el AG difiere dependiendo del sistema de medición. Calcularon el AG medio de sujetos sanos para ocho analizadores (todos ellos con electrodo selectivo de iones).
Las ocho medias oscilaban entre 5,9 mmol/L y 12 mmol/L. Por lo tanto, se descubrió que el intervalo de referencia de 8-16 mmol/L era totalmente apropiado para algunos analizadores, pero demasiado alto para otros.
Es evidente que cada laboratorio debe determinar su propio intervalo de referencia, y los médicos no pueden asumir que el intervalo de referencia tradicional de 8-16 mmol/L, que todavía se cita ampliamente en los textos médicos, es necesariamente apropiado para la interpretación de los resultados de los pacientes en su institución.
DEVOLUCIÓN DEL ANION GAP
El anion gap anormal es un hecho relativamente común entre los pacientes hospitalizados, siendo el aumento del anion gap mucho más común que la reducción del anion gap.
Un estudio retrospectivo de 6868 conjuntos de electrolitos séricos entre pacientes hospitalizados , por ejemplo, reveló que las incidencias del anion gap aumentado y reducido eran del 37,6 % y 2,9 %, respectivamente.
Dado que el cálculo exacto de la brecha aniónica requiere una medición precisa de los electrolitos, los errores aleatorios de laboratorio pueden dar lugar a una brecha aniónica tanto reducida como aumentada. Debe tenerse en cuenta esta posibilidad, si no es evidente una causa patológica para la desviación de la brecha aniónica.
Causas patológicas de la reducción de la brecha aniónica
De la discusión anterior se desprende que la reducción de la brecha aniónica surgirá teóricamente si hay un aumento de los cationes no medidos o una disminución de los aniones no medidos.
A un pH fisiológico, la suma de las cargas negativas de las proteínas normalmente presentes en el suero supera con creces la suma de las cargas positivas, de modo que las proteínas del suero contribuyen de forma significativa a la totalidad de los aniones no medidos y contribuyen de forma insignificante a la totalidad de los cationes no medidos.
De hecho, el 80 % de la brecha aniónica se debe a las proteínas del suero (véase la FIGURA 1). Dado que la albúmina es la más abundante de las proteínas predominantemente aniónicas del suero, no es sorprendente que la reducción de la albúmina sérica (hipoalbuminemia) reduzca la brecha aniónica.
Feldman et al determinaron que por cada 10 g/L de reducción de la albúmina sérica, el gap aniónico del suero se reduce en 2,3 mmol/L.
La hipoalbuminemia es la causa más común de la reducción de la brecha aniónica y algunos han argumentado que en poblaciones de pacientes como los enfermos críticos, que sufren frecuentemente hipoalbuminemia, la corrección de la brecha aniónica sérica para la concentración de albúmina sérica es necesaria para la interpretación precisa de la brecha aniónica sérica.
La acumulación anormal de una proteína sérica individual que tiene una carga positiva neta (catión) tiene el potencial de causar la reducción de la brecha aniónica. La inmunoglobulina IgG es una de estas proteínas catiónicas.
Los pacientes que sufren un mieloma IgG producen grandes cantidades de IgG monoclonal (paraproteína) y, como consecuencia, suelen tener una reducción del gap aniónico. Existe una correlación negativa entre la concentración de paraproteína IgG monoclonal y la brecha aniónica, y en raras ocasiones la brecha aniónica puede tener un valor negativo en pacientes con mieloma IgG. El aumento de la IgG policlonal, sea cual sea su causa, se asocia igualmente a una reducción del anion gap .
Como en el caso de la paraproteinemia IgG monoclonal, cuanto más alta es la IgG, más baja es la brecha aniónica. El aumento de la IgG policlonal es, por ejemplo, la causa de la reducción de la brecha aniónica evidente en pacientes infectados por el VIH.
Teóricamente, el aumento de la concentración sérica de los cationes potasio, calcio o magnesio disminuye la brecha aniónica.
Los aumentos que se observan en la práctica clínica rara vez son suficientes por sí mismos para reducir el gap aniónico por debajo del límite del intervalo de referencia, por lo que la hiperpotasemia, la hipercalcemia y la hipermagnesemia no suelen considerarse en el diagnóstico diferencial del gap aniónico reducido.
Sin embargo, en los pacientes con hipoalbuminemia, y en los pacientes con IgG elevadas, el aumento de cualquiera de estos cationes bien puede contribuir a la reducción de la brecha aniónica.
El catión litio (Li+), que normalmente no está presente en el suero, está presente en el suero de las personas a las que se les prescribe carbonato de litio, un fármaco utilizado para tratar el trastorno bipolar.
La dosis terapéutica se asocia con una concentración de litio en suero de alrededor de 1,0 mmol/L, que no es suficiente para afectar materialmente a la brecha aniónica, pero la sobredosis de litio puede dar lugar a una brecha aniónica reducida o incluso, en casos de intoxicación grave, a una brecha aniónica negativa . Las principales causas de la reducción del gap aniónico se resumen en la TABLA 1.
tabla 1: Causas de anión gap sérico bajo
Las más comunes
Reducción de la albúmina sérica (hipoalbuminemia)
Menos comunes
Paraproteinemia IgG mieloma
Aumento de IgG policonales
Litio
Causa primaria teórica pero rara
Subida del calcio plasmático (hipercalcemia)
Subida del magensio plasmático (hipermagesemia)
Causas patológicas de la elevación del gap aniónico
Teóricamente, el aumento de la brecha aniónica puede ser el resultado de una disminución de cationes no medidos o de un aumento de aniones no medidos. En la práctica es casi exclusivamente el resultado de un aumento de aniones no medidos derivados de los ácidos metabólicos. La acidosis metabólica es, por tanto, la causa más común del aumento de la brecha aniónica.
La principal anomalía que caracteriza a la acidosis metabólica, sea cual sea su causa, es la reducción de la concentración de bicarbonato sérico (HCO3-). Esto puede deberse a una mayor utilización del bicarbonato para amortiguar la acumulación anormal de ácidos, a una mayor pérdida de bicarbonato del organismo o a una regeneración inadecuada del bicarbonato por parte de los riñones.
Para mantener la neutralidad electroquímica, esta reducción del anión medido (bicarbonato) va acompañada de un aumento del cloruro sérico (Cl-), el único otro anión medido, o mucho más comúnmente, de un aumento de aniones no medidos.
En el primer caso, debido a que la reducción del bicarbonato medido se corresponde con el aumento del cloruro medido, la brecha aniónica permanece inalterada y normal; este tipo de acidosis metabólica se denomina acidosis metabólica con brecha aniónica normal (hiperclorémica). En el segundo caso, debido a que hay un aumento de los aniones no medidos, la acidosis metabólica se denomina acidosis metabólica de brecha aniónica aumentada.
La brecha aniónica ha demostrado ser tradicionalmente valiosa en el diagnóstico diferencial de la acidosis metabólica porque, dependiendo de la causa, la acidosis metabólica se asocia con una brecha aniónica elevada o, con mucha menos frecuencia, con una brecha aniónica normal.
Trabajos recientes revisados por Kraut & Madias han revelado que esta utilidad del gap aniónico no es tan clara como se suponía.
El tema principal aquí son las causas de la acidosis metabólica con brecha aniónica aumentada, pero para completar las causas de la acidosis con brecha aniónica normal (hiperclorémica), todas con la excepción de la diarrea bastante rara, se enumeran en la TABLA 2.
Tabla 2: Causas de la acidosis metabólica con brecha aniónica normal (hiperclorémica)
Diarrea
Pancreática, intestinales y biliares
Acidosis del túbulo renal
Ingesta mínima de cloruro (NH4CI)
Insuficiencia suprarrenal (hipoaldosteronismo)
La acumulación anormal de cualquier ácido que no contenga cloruro tiene el potencial de causar un aumento de la acidosis metabólica por brecha aniónica. Como el bicarbonato se consume para amortiguar los protones (catión hidrógeno) del ácido, el anión del ácido se acumula, preservando así la neutralidad electroquímica. Dado que el anión que se acumula «no se mide», la brecha aniónica aumenta.
La acumulación de ácido láctico es probablemente la causa más común de acidosis metabólica. En este caso, la reducción de la concentración de bicarbonato resultante de la amortiguación de protones del ácido láctico se corresponde con un aumento de la concentración del anión «no medido», el lactato.
La acidosis láctica se produce cuando los tejidos se ven privados de oxígeno, por lo que puede surgir en una serie de enfermedades críticas (sepsis, infarto de miocardio, etc.), asociadas al colapso cardiovascular (shock), así como en los traumatismos que implican una importante pérdida de sangre. Varios fármacos, sobre todo las biguanidas, la metformina y la fenformina, así como el alcohol, pueden causar acidosis láctica.
El aumento del lactato es una causa tan común de aumento de la brecha aniónica, especialmente entre los enfermos críticos, que algunos han propuesto que la brecha aniónica fácilmente disponible se utilice como herramienta de detección del aumento del lactato en este grupo de pacientes .
La acumulación anormal de los cetoácidos endógenos, el ácido β-hidroxibutírico y el ácido acetoacético, es la causa de la acidosis metabólica (cetoacidosis) que se produce en la diabetes no tratada y en la inanición, cuando en ausencia de glucosa intracelular se movilizan las grasas como fuente de energía alternativa.
Aquí el aumento de la brecha aniónica se debe al aumento de la concentración sérica de los aniones «no medidos», β-hidroxibutirato y acetoacetato.
La disminución de la excreción de ácidos endógenos y sus aniones es la causa del aumento de la brecha aniónica de la acidosis metabólica que es frecuentemente una característica de la insuficiencia renal.
La intoxicación con etilenglicol y metanol provoca un aumento de la brecha aniónica en virtud de la acidosis metabólica que resulta de su metabolismo a ácido glicólico y fórmico, respectivamente.
La acidosis piroglutámica es una causa poco frecuente, pero probablemente poco reconocida, de la acidosis metabólica por elevación de la brecha aniónica . Kortmann et al informan de tres historias de casos, todos ocurridos en la misma institución en un período de 6 meses.
La relación entre el cambio en la brecha aniónica y el cambio en el bicarbonato (∆AG: ∆HCO3) puede utilizarse para ayudar a identificar las alteraciones ácido-base coexistentes en pacientes con acidosis metabólica.
Esta utilidad del gap aniónico se basa en la noción de que en los casos de aumento puro del gap aniónico, la acidosis metabólica (acidosis láctica, cetoacidosis diabética, etc.), el incremento del gap aniónico con respecto a la normalidad es igual a la disminución del bicarbonato con respecto a la normalidad, de modo que la relación es 1 . Una relación ∆AG: ∆HCO3 de
Una relación de > 1 (aumento del AG mayor que la disminución del bicarbonato) sugiere una alcalosis metabólica coexistente o una acidosis respiratoria coexistente. Kraut & Madias proporciona una revisión crítica de la validez de este uso del gap aniónico.
Aunque la acidosis metabólica es casi invariablemente la causa del aumento marcado del gap aniónico (es decir, AG > 25 mmol/L), no es necesariamente la causa en grados menores de aumento (AG 16-20 mmol/L).
Una serie de otras condiciones pueden dar lugar a un ligero aumento de la brecha aniónica. El aumento de la albúmina sérica (hiperalbuminemia) puede aumentar el anión gap por el mismo mecanismo que la reducción de la albúmina sérica (hipoalbuminemia) reduce el anión gap . Los pequeños aumentos de la brecha aniónica (del orden de 4-6 mmol/L) son evidentes en los pacientes que sufren alcalosis metabólica no complicada por otras alteraciones ácido-base .
Esto ha permitido utilizar el anion gap para ayudar a diferenciar el bicarbonato elevado de la alcalosis metabólica primaria del bicarbonato elevado que surge durante la compensación metabólica de la acidosis respiratoria. En el primer caso, la brecha aniónica está elevada y en el segundo, la brecha aniónica es normal.
Por un mecanismo similar que explica la brecha aniónica reducida en pacientes con mieloma IgG, algunos pacientes con mieloma IgA tienen una brecha aniónica elevada. Esto refleja la observación de que algunas paraproteínas IgA séricas son aniónicas, en contraste con la IgG sérica, que es una proteína catiónica.
Las causas del aumento de la brecha aniónica se enumeran en la TABLA 3.
Tabla 3: Principales causas de elevación del anión gap sérico
Asociada a la acidosis metabólica
Insuficiencia renal
Cetoacidosis diabética
Estarvación
Se trata de un problema de salud pública.
Cetoacidosis alcohólica
Acidosis láctica
Intoxicación por etilenglicol
Intoxicación por metanol
Intoxicación por tolueno
Piroglutámico acidosis (poco frecuente)
Otras afecciones
Aumento de la albúmina sérica (hiperalbuminemia)
Alcalosis metabólica
Mieloma de IgA (no en todos los casos)
La acidosis metabólica es una afección que se produce en la mayoría de los casos.
Resumen
La brecha aniónica es un dato clínico adicional que puede derivarse fácilmente y sin coste del perfil bioquímico más solicitado, urea y electrolitos (U&E). No es posible calcular el gap aniónico si no se incluye el cloruro sérico en el perfil.
El principal uso clínico de la brecha aniónica es la evaluación de las alteraciones ácido-base, en particular la acidosis metabólica. Un aumento marcado de la brecha aniónica (> 25 mmol/L) es casi siempre una prueba irrefutable de acidosis metabólica.
La distinción entre acidosis metabólica normal y de alta brecha aniónica permite que la brecha aniónica ayude a determinar la causa primaria de la acidosis metabólica. La brecha aniónica tiene una utilidad adicional en la investigación de pacientes que presentan acidosis metabólica en asociación con otra alteración ácido-base.
La reducción de la brecha aniónica es, en comparación con el aumento de la brecha aniónica, un hallazgo poco frecuente que no se asocia a una alteración del equilibrio ácido-base, pero que puede ser indicativo de varias afecciones, como la hipoalbuminemia, el mieloma y la intoxicación por litio.
La interpretación precisa de los resultados de la brecha aniónica se ve potencialmente obstaculizada por la falta de consenso sobre el método de cálculo y la significativa variabilidad en el intervalo de referencia.
Un error de laboratorio (ya sea preanalítico o analítico) en la medición de alguno de los tres (o cuatro) parámetros necesarios para realizar el cálculo puede invalidar los resultados del anion gap. Por lo tanto, la brecha aniónica es inusualmente vulnerable a los errores de laboratorio.