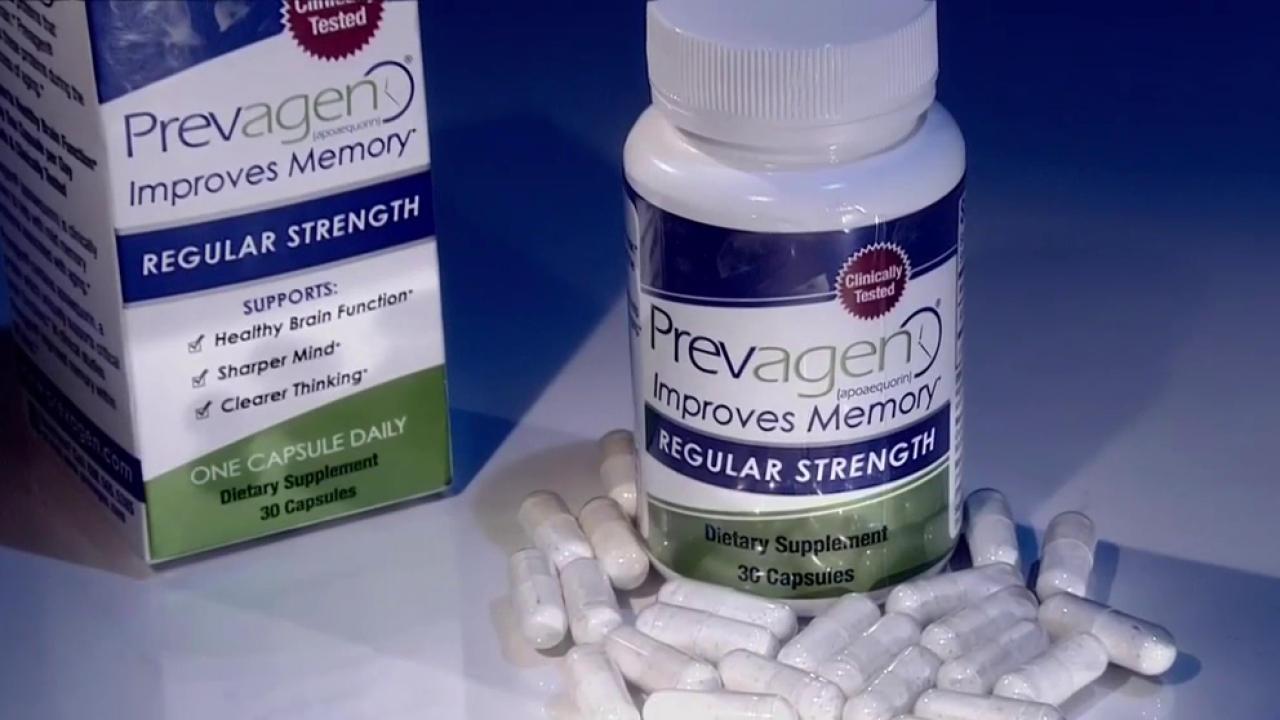
La Federal Trade Commission e il procuratore generale di New York hanno accusato lunedì una società di frode per aver venduto un integratore di memoria basato su una proteina di medusa luminosa.
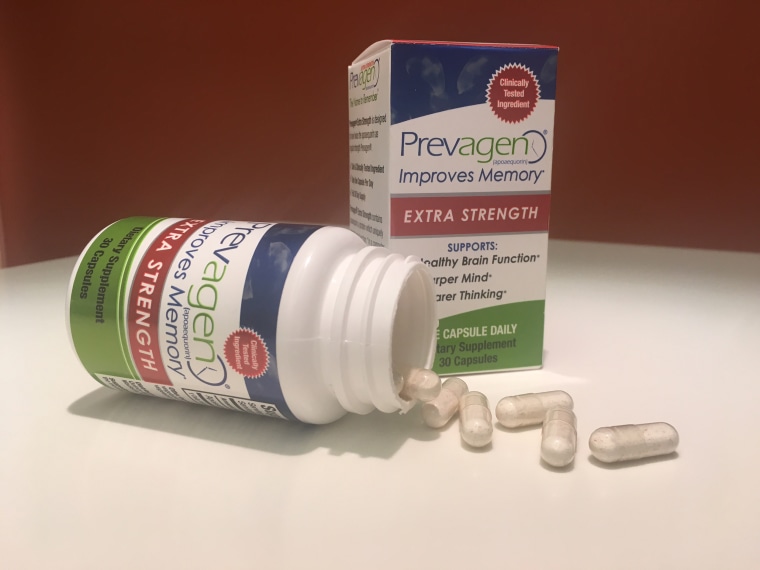
I produttori di un prodotto chiamato Prevagen lo stanno falsamente pubblicizzando come un booster di memoria, e falsamente affermando che il prodotto può entrare nel cervello umano, secondo le accuse.
Ma l’azienda ha risposto duramente, insistendo che il suo prodotto è sicuro e chiamando la FTC è un’agenzia federale “zoppa” con capi che stanno per essere sostituiti dalla prossima amministrazione del presidente eletto Trump.
È l’ultima battaglia in una guerra in corso tra il governo federale e la Quincy Bioscience del Wisconsin. Nel 2012, la Food and Drug Administration ha inviato una lettera di avvertimento alla Quincy, dicendo che stava facendo dichiarazioni mediche per un prodotto che non era passato attraverso il processo formale di approvazione dei farmaci.
Related: Gli integratori mandano migliaia di persone al pronto soccorso
“La Federal Trade Commission e il New York State Attorney General hanno accusato i commercianti dell’integratore alimentare Prevagen di fare affermazioni false e non dimostrate che il prodotto migliora la memoria, fornisce benefici cognitivi ed è clinicamente dimostrato che funziona”, ha detto la FTC in una dichiarazione.
“La vasta campagna pubblicitaria nazionale per Prevagen, compresi gli spot televisivi su reti nazionali e via cavo come CNN, Fox News, e NBC, presentava grafici che descrivevano un rapido e drammatico miglioramento della memoria per gli utenti del prodotto.”
Le capsule, che si vendono tra i 40 e i 90 dollari per una bottiglia, contengono presumibilmente una proteina chiamata apoaequorin, che è fatta da alcune meduse che luminescono.
L’azienda ha cercato, ma non è riuscita, di dimostrare che può aiutare le persone, dice la FTC.
“Il Madison Memory Study non è riuscito a mostrare un miglioramento statisticamente significativo nel gruppo di trattamento.”
“Gli imputati si basano principalmente su uno studio clinico umano in doppio cieco, controllato con placebo, utilizzando misure oggettive di risultato della funzione cognitiva. Questo studio, chiamato Madison Memory Study, ha coinvolto 218 soggetti che assumevano 10 milligrammi di Prevagen o un placebo”, sostiene l’accusa.
“Il Madison Memory Study non è riuscito a mostrare un miglioramento statisticamente significativo nel gruppo di trattamento rispetto al gruppo placebo su nessuno dei nove compiti cognitivi computerizzati.”
L’Alzheimer’s Association non ha voluto pesare sul Prevagen in particolare, ma il responsabile scientifico dell’organizzazione Maria Carrillo ha notato che non c’è nessun prodotto là fuori che sia stato provato per aiutare la memoria.
“L’Alzheimer’s Association ha serie preoccupazioni sulle persone che usano integratori alimentari come alternativa o in aggiunta alle terapie approvate dalla FDA e prescritte dal medico, nel tentativo di trattare o prevenire il morbo di Alzheimer o altre demenze”, ha detto.
“Prima di tutto, l’efficacia e la sicurezza sono sconosciute. Inoltre, la purezza del prodotto è sconosciuta. Infine, gli integratori alimentari possono avere gravi interazioni con i farmaci prescritti.”
Nonostante, l’azienda ha detto che lo studio ha mostrato che il prodotto funziona.
“Gli imputati, tuttavia, non hanno studi che dimostrano che l’apoaequorina somministrata per via orale può attraversare la barriera cerebrale umana e quindi non hanno prove che l’apoaequorina entra nel cervello umano,” secondo l’accusa.
“Non c’è motivo per una FTC a corto di personale e zoppa di affrettare questa denuncia.”
In realtà non importa, perché Prevagen è commercializzato come un integratore.
Il Dietary Supplement Health and Education Act (DSHEA), approvato nel 1994, esenta specificamente le vitamine e gli integratori dal controllo pre-marketing della FDA, anche se l’agenzia può mettere in guardia contro i prodotti ritenuti pericolosi.
Related: Vaccine Advocate Takes on Alternative Medicine Industry
E la FTC, così come il Dipartimento di Giustizia e i funzionari statali, possono agire contro le pratiche di marketing ingannevoli.
“I commercianti di Prevagen hanno sfruttato le paure dei consumatori più anziani che sperimentano la perdita di memoria legata all’età”, ha detto Jessica Rich, direttore del Bureau of Consumer Protection della FTC. “Ma una cosa critica che questi commercianti hanno dimenticato è che le loro affermazioni devono essere sostenute da prove scientifiche reali.”
La causa cerca di multare Quincy e di costringerla a rimborsare i consumatori che hanno comprato le pillole.
“Prima di tutto, l’efficacia e la sicurezza sono sconosciute. Inoltre, la purezza del prodotto è sconosciuta”
Tuttavia, l’azienda ha detto che combatterà le accuse.
“Siamo in forte disaccordo con queste accuse fatte da due soli commissari della FTC. Questo caso è un altro esempio di eccessiva espansione del governo e dei regolatori che estinguono l’innovazione imponendo nuove regole arbitrarie alle piccole imprese come la nostra”, ha detto in una dichiarazione.
“Non c’è motivo per una FTC a corto di personale e zoppa di affrettare questa denuncia.”
I membri del Congresso spesso difendono le aziende. La FDA si è spesso lamentata che il DSHEA permette ai produttori di integratori di vendere prodotti inutili e spesso dannosi ai consumatori fiduciosi, ma il Congresso non è riuscito a rivedere la legislazione.