 Cosa è meglio: una bottiglia di Xalatan da 100 dollari o una bottiglia di latanoprost generico da 25 dollari? Sembra una domanda facile con una risposta ovvia, giusto? Il tuo paziente e il farmacista del paziente possono certamente pensarla così, e non si fanno scrupoli a scegliere il generico molto più economico. Tuttavia, dovreste essere altrettanto attenti ai costi? Dopo tutto, se il generico non funziona correttamente, allora anche i 25 dollari sono uno spreco e la vista del paziente potrebbe essere a rischio.
Cosa è meglio: una bottiglia di Xalatan da 100 dollari o una bottiglia di latanoprost generico da 25 dollari? Sembra una domanda facile con una risposta ovvia, giusto? Il tuo paziente e il farmacista del paziente possono certamente pensarla così, e non si fanno scrupoli a scegliere il generico molto più economico. Tuttavia, dovreste essere altrettanto attenti ai costi? Dopo tutto, se il generico non funziona correttamente, allora anche i 25 dollari sono uno spreco e la vista del paziente potrebbe essere a rischio.
A volte, si ottiene davvero ciò per cui si paga.
D’altra parte, i farmaci generici funzionano abbastanza bene la maggior parte delle volte e offrono risparmi molto reali sui costi, non solo per i singoli pazienti, ma anche per il sistema sanitario nel suo complesso.
Quando è meglio prescrivere il generico o il farmaco di marca? È una domanda che confonde. Ma con un po’ più di informazioni – di cui parleremo in questo articolo – si spera che possiate capire meglio come rispondere a questa domanda per i singoli pazienti.
Basato sulla bioequivalenza
Mentre l’azienda di marca iniziale deve sottoporsi a rigorosi test farmacologici e lunghi studi clinici quando fa domanda alla Food and Drug Administration (FDA), le aziende che producono farmaci generici si sottopongono semplicemente a una forma abbreviata del processo di approvazione. La sicurezza e l’efficacia non devono essere provate o stabilite con i generici perché i test approfonditi sul farmaco di marca sono presumibilmente già stati condotti. Le aziende devono semplicemente dimostrare alla FDA che i loro farmaci sono bioequivalenti al marchio.1 Attualmente, per dimostrare la bioequivalenza, gli scienziati devono dimostrare che il generico si trova in una gamma accettabile +/- della concentrazione etichettata. In genere, questo si ottiene assicurando che la versione generica rilasci il suo principio attivo nel flusso sanguigno alla stessa velocità e nella stessa quantità del farmaco di marca.1
Mentre questo è relativamente facile da misurare con i farmaci sistemici, la bioequivalenza dei farmaci oftalmici non può essere testata in modo affidabile allo stesso modo. Inoltre, le concentrazioni nel sangue di un farmaco oftalmico applicato direttamente all’occhio non sono probabilmente importanti nella valutazione della sua efficacia. Quindi, l’unica stipulazione della FDA per i farmaci generici oftalmici è che contengano la stessa concentrazione del principio attivo, il dosaggio e la via di somministrazione.2
Senza un vero test di bioequivalenza per i farmaci oftalmici, gli oculisti devono presumere che funzionino ugualmente bene; tuttavia, sappiamo tutti che questo non è sempre il caso. La maggior parte degli oculisti probabilmente ricorda la serie di pazienti nei primi anni 2000 che hanno sperimentato la fusione della cornea associata all’uso della soluzione oftalmica di diclofenac generico (rispetto al Voltaren di marca) dopo la chirurgia oculare. In un articolo, tre pazienti su cinque che hanno sperimentato una fusione corneale stavano prendendo diclofenac generico, e quattro pazienti alla fine sono progrediti fino alla perforazione corneale che ha richiesto un trapianto.3
Problemi potenziali con i generici
I medici e gli analisti di politica sanitaria concordano ampiamente sul fatto che i farmaci generici possono portare un risparmio significativo ai costi sanitari. Uno studio del 2002 dello Schneider Institute for Health Policy della Brandeis University ha indicato che se l’uso dei generici fosse aumentato tra i beneficiari di Medicare, ci potrebbe essere un risparmio teorico di miliardi di dollari per l’assistenza sanitaria.4 Un rapporto del 2005 ha stimato che per ogni 1% di aumento nell’uso dei farmaci generici, la spesa complessiva per i farmaci da prescrizione sarebbe ridotta tra 1,3 e 4 miliardi di dollari all’anno.5
D’altra parte, è possibile che le visite di controllo del medico possano aumentare in numero e/o frequenza se la compagnia di assicurazione o il paziente decide di passare ai farmaci generici. Questo potrebbe effettivamente annullare il risparmio sanitario.
Soprattutto con i farmaci per il glaucoma, alcuni medici potrebbero essere più inclini a riportare i pazienti prima per controllare l’efficacia e la tollerabilità del farmaco generico rispetto a quanto farebbero normalmente se non ci fosse stato il passaggio. A causa del numero crescente di produttori di generici e del potenziale di efficacia differente tra i generici, uno specialista di glaucoma è arrivato al punto di raccomandare di tracciare ogni tipo di generico facendo portare ai pazienti i flaconi ad ogni visita. In questo modo, può seguire ogni tipo di generico e osservare i modelli di efficacia e tollerabilità.6
Mentre la FDA stabilisce le linee guida definitive per i farmaci generici prodotti negli Stati Uniti, le fabbriche di produzione all’estero non possono essere monitorate così attentamente. Anche se la domanda di un’azienda alla FDA deve includere una descrizione completa delle strutture che utilizza per la produzione, i test e il confezionamento, ci possono essere restrizioni di bilancio che impediscono ad ogni struttura all’estero di essere ispezionata con lo stesso programma di quelle negli Stati Uniti.7
C’è anche preoccupazione per gli ingredienti dei farmaci generici provenienti da possibili fonti con meno controlli, come India e Cina. Per esempio, uno studio del 2005 ha scoperto che il 20% dei colliri generici di ciprofloxacina acquistati in India erano sottopotenti, e alcune preparazioni del contenuto antibiotico erano abbastanza basse da influenzare negativamente i risultati del trattamento.8
Con i farmaci generici, un aumento dei sintomi di allergia da un mese all’altro può verificarsi se c’è una differenza tra i produttori nei conservanti e/o negli ingredienti inattivi che usano. Se la farmacia riceve il farmaco da aziende diverse di mese in mese, questo potrebbe potenzialmente comportare una maggiore tossicità della superficie oculare, una scarsa tollerabilità e il ritorno dei pazienti per una visita con gli “occhi rossi”.
Basta guardare indietro ai problemi relativi al Travatan (travoprost, Alcon) conservato con cloruro di benzalconio (BAK) per vedere la possibilità di problemi con alcuni conservanti.9 Come precedentemente notato, i farmaci generici devono avere solo la stessa concentrazione di principio attivo, il che significa che gli ingredienti inattivi e i conservanti sono spesso diversi. Di conseguenza, un maggior numero di visite in ufficio per controllare l’efficacia e la tollerabilità di un farmaco generico potrebbe teoricamente causare un aumento dei costi delle cure oculistiche, e compensare il risparmio derivante dal prezzo più basso del farmaco.6
Il numero crescente di produttori di farmaci generici può portare a un aspetto incoerente dei flaconi e a una maggiore incertezza del paziente sulla corretta conformità. I produttori di farmaci generici devono seguire gli standard di produzione e rispettare i regolamenti di etichettatura, che vietano che i flaconi di farmaci generici abbiano un aspetto simile alle loro controparti di marca.10 Questo può causare confusione tra i pazienti se c’è un diverso colore del tappo, un diverso colore dell’etichetta o una dimensione del flacone che varia di mese in mese. Uno studio ha scoperto che il 36% delle persone ha detto che sarebbe stato turbato o preoccupato se il colore o l’aspetto del loro flacone di medicinali fosse cambiato in qualsiasi forma.11
Alcuni medicinali generici hanno anche scoperto di avere diverse dimensioni del contagocce, che possono variare la dimensione della goccia, il numero di dosi nel contenitore, e in definitiva il costo di una fornitura mensile.12 Inoltre, sono state espresse preoccupazioni sulla plastica utilizzata nei flaconi dei farmaci e sul controllo di qualità e su ciò che questo significa in termini di efficacia.6
Dobbiamo riconoscere l’importanza del nostro ruolo nell’educazione del paziente riguardo a queste potenziali differenze e assicurarci che i nostri pazienti ci contattino se hanno domande sul loro trattamento.
Studi sui generici – Gocce per glaucoma. Attualmente, il farmaco oftalmico generico che fa più notizia è il latanoprost 0,005%, la versione commerciale di Xalatan (Pfizer). Attualmente, “The Orange Book”, il testo della FDA contenente “Approved Drug Products with Therapeutic Equivalence”, elenca sette produttori approvati di latanoprost generico.13
– Gocce per glaucoma. Attualmente, il farmaco oftalmico generico che fa più notizia è il latanoprost 0,005%, la versione commerciale di Xalatan (Pfizer). Attualmente, “The Orange Book”, il testo della FDA contenente “Approved Drug Products with Therapeutic Equivalence”, elenca sette produttori approvati di latanoprost generico.13
L’efficacia dei farmaci generici per il glaucoma è di particolare interesse nella comunità oftalmica. Anche se il generico può essere meno costoso e può fornire un risparmio significativo, c’è una certa preoccupazione che i farmaci generici per il glaucoma non abbiano lo stesso effetto delle loro versioni commerciali, e il risultato potrebbe essere la progressione della malattia e la perdita della vista.14
Tuttavia, un recente studio che ha confrontato il latanoprost generico con lo Xalatan ha rilevato che entrambi i trattamenti hanno dimostrato una sicurezza e una tollerabilità comparabili tra i pazienti.15 Da notare, però, che il 99,6% dei pazienti nello studio erano bianchi, quindi questi risultati potrebbero non essere gli stessi negli afroamericani, asiatici e ispanici. Inoltre, si potrebbe sostenere che ci può essere stato un pregiudizio del ricercatore perché Bausch + Lomb, il produttore del generico, ha condotto lo studio.
In precedenza, c’era stato solo un altro studio condotto su una formulazione generica di latanoprost nel 2007.16 Lo studio consisteva di 30 pazienti che sono stati randomizzati in due gruppi; hanno ricevuto Xalatan o un generico latanoprost (Latoprost, prodotto in India) per le prime 12 settimane, poi sono passati all’altro farmaco per le ultime 12 settimane. I ricercatori hanno scoperto che i pazienti che sono stati passati da Latoprost a Xalatan hanno sperimentato un’ulteriore diminuzione della IOP. Al contrario, quando i soggetti sono passati da Xalatan a Latoprost, la IOP è aumentata in media di più di 1 mm Hg. Nel complesso, il generico, che è formulato a un pH più alto rispetto al prodotto di marca, è risultato meno efficace nell’abbassare la IOP.16
Almeno uno studio ha scoperto che il prednisolone acetato generico ha particelle molto più grandi, che si depositano fuori dalla sospensione a una velocità maggiore, affondano sul fondo e richiedono una maggiore agitazione da parte del paziente.
Sono state sollevate preoccupazioni anche riguardo alla prescrizione della versione generica del timololo in forma di gel. I ricercatori hanno dimostrato che il tempo di ritenzione sulla superficie oculare differisce tra i vari veicoli di gel a rilascio prolungato. In particolare, la gomma di gellano presente nel Timoptic-XE (timololo maleato soluzione oftalmica in forma di gel, Merck) può consentire al farmaco di marca di avere una superficie di contatto più lunga, un migliore assorbimento e un’attività beta-bloccante intraoculare.17 In uno studio del 2002, la versione di marca di timololo soluzione in gel a base di gomma di gellano ha dimostrato di abbassare la IOP meglio della sua controparte generica a base di gomma di xantano.18 Di conseguenza, alcuni individui nel campo medico hanno proposto che considerazioni come la dimensione delle particelle e altre proprietà di una sospensione devono essere valutate per l’equivalenza generica.19
– Gocce steroidee. Diversi studi e casi negli ultimi anni hanno anche illustrato la necessità di esercitare cautela e vigilanza quando si trattano infiammazioni con steroidi oftalmici. Allergan ha notato nei suoi memorandum ai medici che la sospensione microfine del suo Pred Forte (prednisolone acetato) è più uniforme, rimane più a lungo nel sacco congiuntivale e riduce al minimo l’irritazione meccanica dell’occhio rispetto al prednisolone acetato generico.20
Uno studio del 2007 ha esaminato le differenze nella dimensione delle particelle tra Pred Forte, EconoPred Plus e il prednisolone acetato generico all’1%.21 L’ipotesi era che le particelle più grandi si sarebbero depositate fuori dalla sospensione più velocemente, sarebbero affondate sul fondo e avrebbero richiesto una maggiore agitazione da parte del paziente. I risultati dello studio hanno rilevato che la forma generica di prednisolone acetato aveva una maggiore tendenza all’agglomerazione delle particelle, che di conseguenza portava a una concentrazione di dosaggio incoerente.21 Inoltre, gli autori hanno scritto che le particelle di dimensioni maggiori possono potenzialmente ostruire la punta del flacone del farmaco durante l’instillazione e alterare ulteriormente la consistenza e la concentrazione del dosaggio. Al contrario, le dimensioni delle particelle in Pred Forte erano più piccole e più uniformi, il che ha permesso loro di rimanere in sospensione più a lungo e ha dato un dosaggio più preciso della goccia.21
Gli optometristi dovrebbero considerare che i prodotti con ingredienti mal sospesi possono potenzialmente compromettere il trattamento di occhi altamente infiammati.
Persona del paziente
– Costo e conformità. Teoricamente, i farmaci generici dovrebbero migliorare la gestione e la compliance del paziente perché l’ostacolo del costo è stato rimosso. Con un analogo della prostaglandina più accessibile ora disponibile, i pazienti che prima prendevano timololo generico, dorzolamide generica o quelli che hanno rifiutato il trattamento possono scegliere di prendere latanoprost generico. Questo tipo di passaggio tra le classi di farmaci per il glaucoma dovrebbe anche portare a una conformità significativamente maggiore, grazie al programma di dosaggio giornaliero della prostaglandina.
– Complesso di inferiorità. Un altro potenziale problema è che i pazienti possono essere resistenti ad assumere un farmaco generico perché li percepiscono come inferiori alla loro controparte di marca.22 I generici sono spesso considerati farmaci di seconda scelta a causa della percezione di una scarsa conformità alle pratiche di produzione standard, della mancanza di conoscenza dei pazienti sui generici e dell’influenza dell’azienda di marca.22,23 Secondo uno studio in Nuova Zelanda, meno della metà dei partecipanti intervistati percepisce i farmaci generici come sicuri, efficaci e di pari qualità rispetto alla loro controparte di marca.11
Inoltre, lo studio neozelandese ha scoperto che i pazienti più giovani che avevano una migliore conoscenza e comprensione delle differenze dei farmaci erano più propensi di quelli con scarsa comprensione dei farmaci a dire che avrebbero usato un farmaco generico sia nelle malattie maggiori che in quelle minori.11 Dobbiamo educare i nostri pazienti in modo che possano prendere una decisione informata sul loro trattamento ed essere disposti a provare un farmaco generico se la situazione è appropriata. Questo è particolarmente vero negli anziani che possono assumere più farmaci, così come quelli con uno status socioeconomico basso che potrebbero beneficiare del risparmio.
– Preferenze del paziente. Spesso dobbiamo considerare la personalità del nostro paziente e le sue esperienze passate quando decidiamo tra farmaci generici e di marca. Una domanda importante da fare ai nostri pazienti è se hanno preso dei generici in precedenza e qual è stato il risultato. Se il paziente ha avuto una cattiva esperienza, potrebbe essere orientato verso i farmaci di marca e disposto a pagare il prezzo più alto.
La gravità della malattia può anche influenzare la disponibilità del paziente a prendere un farmaco generico. Secondo lo stesso studio in Nuova Zelanda, le persone intervistate erano più disposte a passare a un generico per una malattia minore che per una malattia maggiore (79% contro 58,7%).11 In una malattia grave come il glaucoma, che ha il potenziale per una perdita permanente della vista, i pazienti possono essere meno disposti a passare a un generico.
A quale storia credere?
La vera sicurezza ed efficacia dei farmaci generici non può essere certa senza studi clinici testa a testa che confrontino i farmaci oftalmici topici di marca con le loro controparti generiche, ma attualmente i dati sono limitati.19 Per ora, ecco cosa facciamo:
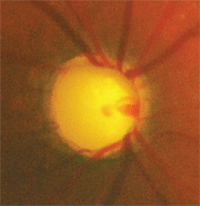
Un paziente con glaucoma avanzato o allo stadio finale, che è ad alto rischio di progressione e perdita della vista, dovrebbe probabilmente continuare con i farmaci di marca per mantenere la PIO sotto controllo.
Nei pazienti con infiammazione oculare secondaria all’irite, data la ricerca di cui sopra, preferiamo prescrivere Pred Forte piuttosto che un generico quando possibile.
Analogamente, a causa della mancanza di informazioni sull’efficacia dei farmaci generici per il glaucoma, nei pazienti con glaucoma avanzato o allo stadio finale che sono ad alto rischio di progressione e di perdita della vista, prendiamo in forte considerazione la possibilità di rimanere con il farmaco di marca che ha la IOP del paziente sotto buon controllo. Non vogliamo rischiare di perdere il controllo della malattia o di causare tossicità oculare passando dal marchio al generico.
Preparare una lettera di riserva per la compagnia di assicurazione, in cui si dichiara che il vostro paziente ha un “glaucoma avanzato o in fase terminale che minaccia la vista” ed è stato stabile con i suoi farmaci attuali, sarà utile se e quando si presenta questa situazione. Un’altra opzione è quella di passare i pazienti a un farmaco di marca per il quale non è disponibile un generico in quel momento (ad esempio, passare il paziente da Xalatan a un’altra prostaglandina di marca), a condizione di ottenere un’efficacia simile.
In generale, dobbiamo educare i nostri pazienti sul potenziale di allergia e scarsa efficacia dei farmaci generici. Inoltre, potrebbero essere necessarie più visite in ufficio per valutare l’effetto di abbassamento della IOP tra i farmaci per il glaucoma generici e di marca, così come altri farmaci oftalmici.
Inoltre, dobbiamo dire ai pazienti di contattarci se sperimentano effetti avversi dopo il passaggio a un farmaco generico. Finché l’efficacia è comparabile e non ci sono reazioni allergiche, i generici forniscono un’opzione di trattamento alternativo accessibile che dovrebbe essere utilizzata e prescritta ai nostri pazienti.
Come fornitori di cure oculistiche, dobbiamo ricordare che quando si sceglie tra farmaci generici e di marca, ci sono due lati della storia.
Il dottor Chu e il dottor Hamp vedono grandi popolazioni di pazienti con malattia avanzata. Entrambi tengono conferenze sul glaucoma e su altri argomenti clinici. Non hanno interessi finanziari o proprietari in nessuno dei suddetti farmaci e/o aziende.
1. Cantor LB. Processo di approvazione dei farmaci generici oftalmici: implicazioni per l’efficacia e la sicurezza. J Glaucoma. 1997 Oct;6(5):344-9.
2. Fiscella RG. Pesare la scelta tra farmaci generici e di marca. Inserto a Cat Refr Surg Today. 2010 giugno. Disponibile presso: http://bmctoday.net/crstoday/2010/06/insert/article.asp?f=weighing-the-choice-between-generic-and-branded-drugs (accesso gennaio 2012).
3. Lin JC, Rapuano CJ, Laibson PR, et al. Fusione corneale associata all’uso di farmaci antinfiammatori non steroidei topici dopo chirurgia oculare. Arch Ophthalmol. 2000 Aug;118(8):1129-32.
4. U.S. Food and Drug Administration. Maggiore accesso ai farmaci generici: Nuove iniziative della FDA per migliorare il processo di revisione dei farmaci e ridurre le scappatoie legali. Gennaio 2006. Disponibile all’indirizzo: www.fda.gov/drugs/resourcesforyou/consumers/ucm143545.htm (accesso gennaio 2012).
5. Sottocommissione per la salute del Comitato per l’energia e il commercio Audizione, Camera dei rappresentanti, 109° Congresso. Aumentare l’utilizzo di farmaci generici: Risparmiare denaro per i pazienti. 18 maggio 2005. Disponibile su: www.gpo.gov/fdsys/pkg/CHRG-109hhrg21639/pdf/CHRG-109hhrg21639.pdf (accesso gennaio 2012).
6. Loewen NA, Realini T, Ruderman JM, Smit B. Xalatan va generico: un evento storico nel glaucoma. Glaucoma Oggi. Inizio estate 2011:55-8.
7. U.S. Food and Drug Administration. FDA garantisce l’equivalenza dei farmaci generici. Disponibile all’indirizzo: www.fda.gov/Drugs/EmergencyPreparedness/BioterrorismandDrugPreparedness/ucm134444.htm (accesso gennaio 2012).
8. Weir RE, Zaidi FH, Charteris DG, et al. Variabilità nel contenuto di ciprofloxacina generico indiano collirio. Br J Ophthalmol. 2005 Sep;89(9):1094-6.
9. Baudouin C, Riancho L, Warnet JM, et al. Studi in vitro di analoghi delle prostaglandine antiglaucomatose: travoprost con e senza cloruro di benzalconio e latanoprost conservato. Invest Ophthalmol Vis Sci. 2007 Sep;48(9):4123-8.
10. Gallardo MJ, Fiscella RG, Whitson JT. Farmaci generici per il glaucoma. Glaucoma Oggi. 2006 Jan-Feb;4(1):32-5.
11. Babar ZU, Stewart J, Reddy S, et al. Una valutazione delle conoscenze, percezioni e atteggiamenti dei consumatori riguardo ai farmaci generici a Auckland. Pharm World Sci. 2010 Aug;32(4):440-8.
12. Kirkner RM. Miti e realtà del latanoprost generico. Ufficio oftalmico. 2011 giugno.
13. U.S. Food and Drug Administration. Libro Arancione: Prodotti farmaceutici approvati con valutazioni di equivalenza terapeutica. Ultimo aggiornamento: 28 ottobre 2011. Disponibile all’indirizzo: www.accessdata.fda.gov/scripts/cder/ob/default.cfm (accesso gennaio 2012).
14. Bell NP, Ramos JL, Feldman RM. Sicurezza, tollerabilità ed efficacia della terapia di combinazione fissa con dorzolamide hydrocholoride 2% e timololo maleato 0,5% nel glaucoma e nell’ipertensione oculare. Clin Ophthalmol. 2010 Nov 22;4:1331-46.
15. Allaire C, Dietrich A, Allmeier H, et al. Latanoprost 0,005% formulazione di prova è efficace come Xalatan in pazienti con ipertensione oculare e glaucoma primario ad angolo aperto. Eur J Ophthalmol. 2012 Jan;22(1):19-27.
16. Narayanaswamy A, Neog A, Baskaran M, et al. Uno studio pilota randomizzato, crossover, open label per valutare l’efficacia e la sicurezza di Xalatan in confronto con latanoprost generico (Latoprost) in soggetti con glaucoma primario ad angolo aperto o ipertensione oculare. Indian J Ophthalmol. 2007 Mar-Apr;55(2):127-31.
17. Meseguer G, Buri P, Plazonnet B, et al. Confronto gamma scintigrafico di colliri contenenti pilocarpina in volontari sani. J Ocul Pharmacol Ther. 1996 Winter;12(4):481-8.
18. Stewart WC, Sharpe ED, Stewart JA, Hott CE. La sicurezza e l’efficacia del timololo 0,5% in gomma xantana rispetto al timololo in soluzione formante gel 0,5%. Curr Eye Res. 2002 maggio;24(5):387-91.
19. Fiscella RG, Gaynes BI, Jensen M. Equivalenza dei prodotti oftalmici generici e di marca. Am J Health Syst Pharm. 2001 Apr 1;58(7):616-7.
20. Allergan Medical Affairs. Informazioni mediche sulle gocce oftalmiche Prednisolone Forte. Irvine, CA, comunicazione del 19 dicembre 2011.
21. Roberts CW, Nelson PL. Analisi comparativa delle sospensioni di prednisolone acetato. J Ocul Pharmacol Ther. 2007 Apr;23(2):182-7.
22. King DR, Kanavos P. Incoraggiare l’uso di farmaci generici: implicazioni per le economie di transizione. Croat Med J. 2002 Aug;43(4):462-9.
23. Verbale della riunione del Comitato consultivo dei consumatori PHARMAC (CAC), 13 luglio 2007; Wellington, Nuova Zelanda. Disponibile su: www.pharmac.govt.nz/pdf/021007a.pdf (accesso gennaio 2012).
24. Pharmaceutical Research and Manufacturers of America. Comunicato stampa: R&D Gli investimenti delle aziende biofarmaceutiche statunitensi hanno raggiunto livelli record nel 2010. 15 marzo 2011; Washington, D.C. Disponibile su: www.phrma.org/media/releases/rd-investment-us-biopharmaceutical-companies-reached-record-levels-2010 (accesso gennaio 2012).