Les résultats d’apprentissage
- Lister les applications courantes des isotopes radioactifs
Les isotopes radioactifs ont les mêmes propriétés chimiques que les isotopes stables du même élément, mais ils émettent un rayonnement, qui peut être détecté. Si nous remplaçons un (ou plusieurs) atome(s) par un (des) radio-isotope(s) dans un composé, nous pouvons les suivre en surveillant leurs émissions radioactives. Ce type de composé est appelé traceur radioactif (ou marqueur radioactif). Les radio-isotopes sont utilisés pour suivre le déroulement des réactions biochimiques ou pour déterminer comment une substance est distribuée dans un organisme. Les traceurs radioactifs sont également utilisés dans de nombreuses applications médicales, tant pour le diagnostic que pour le traitement. Ils servent à mesurer l’usure des moteurs, à analyser la formation géologique autour des puits de pétrole, et bien plus encore.
Les radio-isotopes ont révolutionné la pratique médicale (voir Demi-vies de plusieurs isotopes radioactifs), où ils sont largement utilisés. Plus de 10 millions de procédures de médecine nucléaire et plus de 100 millions de tests de médecine nucléaire sont réalisés chaque année aux États-Unis. Quatre exemples typiques de traceurs radioactifs utilisés en médecine sont le technétium-99 \left({}_{43}^{99}\text{Tc}\right), le thallium-201 \left({}_{81}^{201}\text{Tl}\right), l’iode-131 \left({}_{53}^{131}\text{I}\right), et le sodium-24 \left({}_{11}^{24}\text{Na}\right). Les tissus endommagés du cœur, du foie et des poumons absorbent préférentiellement certains composés du technétium-99. Après son injection, la localisation du composé de technétium, et donc du tissu endommagé, peut être déterminée en détectant les rayons γ émis par l’isotope Tc-99. Le thallium-201 se concentre dans les tissus cardiaques sains, de sorte que les deux isotopes, le Tc-99 et le Tl-201, sont utilisés ensemble pour étudier les tissus cardiaques. L’iode-131 se concentre dans la glande thyroïde, le foie et certaines parties du cerveau. Il peut donc être utilisé pour surveiller le goitre et traiter les troubles de la thyroïde, comme la maladie de Grave, ainsi que les tumeurs du foie et du cerveau. Des solutions salines contenant des composés de sodium-24 sont injectées dans le sang pour aider à localiser les obstructions à la circulation sanguine.

Figure 1. L’administration de thallium-201 à un patient et la réalisation ultérieure d’une épreuve d’effort offrent aux professionnels médicaux la possibilité d’analyser visuellement la fonction cardiaque et le flux sanguin. (crédit : modification du travail de « Blue0ctane »/Wikimedia Commons)
Les radio-isotopes utilisés en médecine ont généralement une demi-vie courte – par exemple, l’omniprésent Tc-99m a une demi-vie de 6,01 heures. Le Tc-99m est donc impossible à stocker et son coût de transport est prohibitif ; il est donc fabriqué sur place. Les hôpitaux et autres installations médicales utilisent le Mo-99 (qui est principalement extrait des produits de fission de l’U-235) pour générer le Tc-99. Le Mo-99 subit une désintégration β avec une demi-vie de 66 heures, et le Tc-99 est ensuite extrait chimiquement. Le nucléide parent Mo-99 fait partie d’un ion molybdate, {\text{MoO}}_{4}^{2-} ; lorsqu’il se désintègre, il forme l’ion pertechnétate, {\text{TcO}}_{4}^{\text{-}}. Ces deux ions hydrosolubles sont séparés par chromatographie sur colonne, l’ion molybdate de charge supérieure s’adsorbant sur l’alumine de la colonne, et l’ion pertechnétate de charge inférieure traversant la colonne dans la solution. Quelques microgrammes de Mo-99 peuvent produire suffisamment de Tc-99 pour réaliser jusqu’à 10 000 tests.

Figure 2. (a) Le premier générateur de Tc-99m (vers 1958) est utilisé pour séparer le Tc-99 du Mo-99. Le MoO42- est retenu par la matrice dans la colonne, tandis que le TcO4- passe à travers et est collecté. (b) Le Tc-99 a été utilisé dans ce scanner du cou d’un patient atteint de la maladie de Grave. Le scanner montre l’emplacement des fortes concentrations de Tc-99. (crédit a : modification du travail par le Département de l’énergie ; crédit b : modification du travail par « MBq »/Wikimedia Commons)
Les radio-isotopes peuvent également être utilisés, généralement à des doses plus élevées que celles utilisées comme traceur, comme traitement. La radiothérapie consiste à utiliser des rayonnements à haute énergie pour endommager l’ADN des cellules cancéreuses, ce qui les tue ou les empêche de se diviser. Un patient cancéreux peut recevoir une radiothérapie externe délivrée par une machine située à l’extérieur du corps, ou une radiothérapie interne (curiethérapie) à partir d’une substance radioactive introduite dans le corps. Notez que la chimiothérapie est similaire à la radiothérapie interne dans la mesure où le traitement contre le cancer est injecté dans le corps, mais diffère en ce que la chimiothérapie utilise des substances chimiques plutôt que radioactives pour tuer les cellules cancéreuses.

Figure 3. Le dessin humoristique en (a) montre une machine au cobalt 60 utilisée dans le traitement du cancer. Le diagramme en (b) montre comment le portique de la machine à Co-60 se balance en arc de cercle, concentrant le rayonnement sur la région ciblée (tumeur) et minimisant la quantité de rayonnement qui traverse les régions voisines.
Le cobalt-60 est un radio-isotope synthétique produit par l’activation neutronique du Co-59, qui subit ensuite une désintégration β pour former le Ni-60, ainsi que l’émission d’un rayonnement γ. Le processus global est le suivant :
{}_{27}^{59}\text{Co}+{}_{0}^{1}\text{n}\longrightarrow {}_{27}^{60}\text{Co}\longrightarrow {}_{28}^{60}\text{Ni}+{}_{-1}^{0}\beta+2{}_{0}^{0}\gamma
Le schéma global de désintégration de ce dernier est représenté graphiquement sur la figure 4.

Figure 4. Le Co-60 subit une série de désintégrations radioactives. Les émissions γ sont utilisées pour la radiothérapie.
Les radio-isotopes sont utilisés de diverses manières pour étudier les mécanismes des réactions chimiques chez les plantes et les animaux. Il s’agit notamment du marquage des engrais dans les études sur l’absorption des nutriments par les plantes et la croissance des cultures, des enquêtes sur les processus de digestion et de production de lait chez les vaches, et des études sur la croissance et le métabolisme des animaux et des plantes.
Par exemple, le radio-isotope C-14 a été utilisé pour élucider les détails du déroulement de la photosynthèse. La réaction globale est la suivante :
{\text{6CO}}_{2}\left(g\right)+{\text{6H}}_{2}\text{O}\left(l\right)\longrightarrow {\text{C}}_{6}{\text{H}}_{12}{\text{O}}_{6}\left(s\right)+{\text{6O}}_{2}\left(g\right),
mais le processus est beaucoup plus complexe, procédant par une série d’étapes au cours desquelles divers composés organiques sont produits. Dans le cadre d’études sur le déroulement de cette réaction, des plantes ont été exposées à du CO2 contenant une forte concentration de {}_{6}^{14}\text{C}. À intervalles réguliers, les plantes ont été analysées pour déterminer quels composés organiques contenaient du carbone 14 et quelle quantité de chaque composé était présente. À partir de la séquence temporelle dans laquelle les composés sont apparus et de la quantité de chacun d’eux présente à des intervalles de temps donnés, les scientifiques en ont appris davantage sur la voie de la réaction.
Les applications commerciales des matériaux radioactifs sont tout aussi diverses. Elles consistent notamment à déterminer l’épaisseur des films et des feuilles métalliques minces en exploitant le pouvoir de pénétration de divers types de rayonnement. Les défauts des métaux utilisés à des fins structurelles peuvent être détectés à l’aide des rayons gamma à haute énergie du cobalt 60, d’une manière similaire à la façon dont les rayons X sont utilisés pour examiner le corps humain. Dans une forme de lutte contre les parasites, les mouches sont contrôlées en stérilisant les mouches mâles avec un rayonnement γ afin que les femelles qui s’accouplent avec eux ne produisent pas de progéniture. De nombreux aliments sont conservés par des rayonnements qui tuent les micro-organismes à l’origine de la détérioration des aliments.

Figure 5. Les utilisations commerciales courantes des rayonnements comprennent (a) l’examen aux rayons X des bagages dans un aéroport et (b) la conservation des aliments. (crédit a : modification des travaux du ministère de la Marine ; crédit b : modification des travaux du ministère américain de l’Agriculture)
L’Américium-241, un émetteur α dont la demi-vie est de 458 ans, est utilisé en quantités infimes dans les détecteurs de fumée de type ionisation. Les émissions α de l’Am-241 ionisent l’air entre deux plaques d’électrodes dans la chambre d’ionisation. Une batterie fournit un potentiel qui provoque le mouvement des ions, créant ainsi un petit courant électrique. Lorsque de la fumée pénètre dans la chambre, le mouvement des ions est entravé, ce qui réduit la conductivité de l’air. Cela provoque une baisse marquée du courant, déclenchant une alarme.
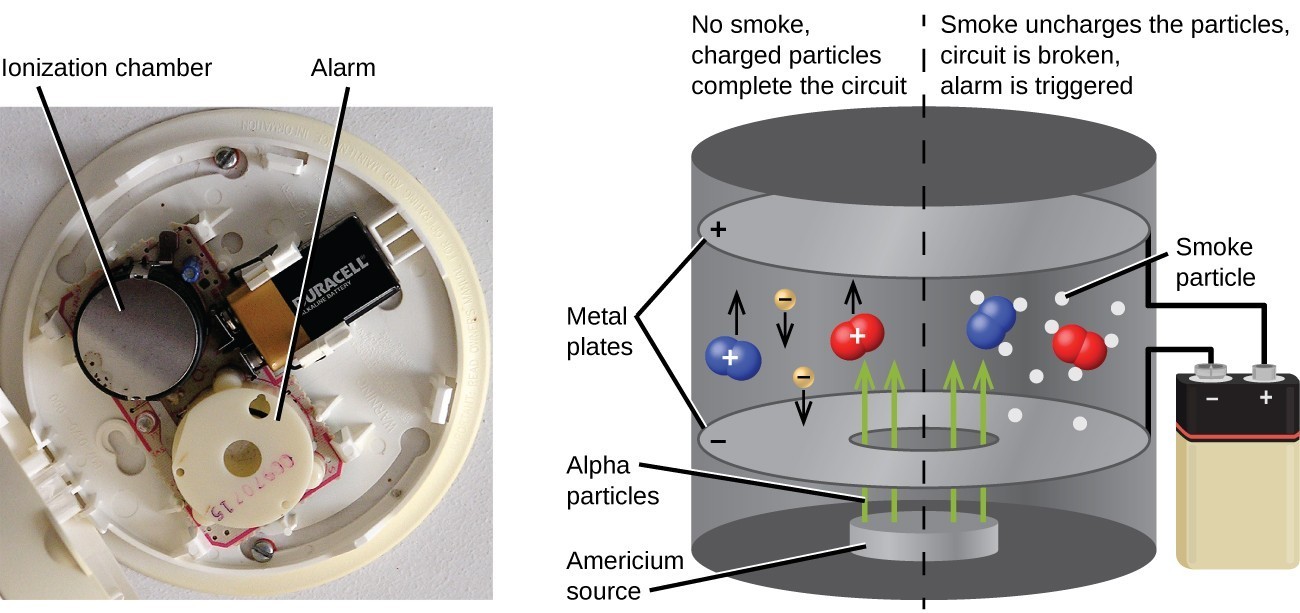
Figure 6. À l’intérieur d’un détecteur de fumée, l’Am-241 émet des particules α qui ionisent l’air, créant un petit courant électrique. Lors d’un incendie, les particules de fumée entravent le flux d’ions, réduisant le courant et déclenchant une alarme. (crédit a : modification du travail de « Muffet »/Wikimedia Commons)
Concepts clés et résumé
Les composés connus sous le nom de traceurs radioactifs peuvent être utilisés pour suivre des réactions, suivre la distribution d’une substance, diagnostiquer et traiter des conditions médicales, et bien plus encore. D’autres substances radioactives sont utiles pour lutter contre les parasites, visualiser des structures, donner des alertes incendie, et pour de nombreuses autres applications. Des centaines de millions de tests et de procédures de médecine nucléaire, utilisant une grande variété de radio-isotopes aux demi-vies relativement courtes, sont réalisés chaque année aux États-Unis. La plupart de ces radio-isotopes ont des demi-vies relativement courtes ; certaines sont suffisamment courtes pour que le radio-isotope doive être fabriqué sur place dans les établissements médicaux. La radiothérapie utilise des rayonnements à haute énergie pour tuer les cellules cancéreuses en endommageant leur ADN. Les rayonnements utilisés pour ce traitement peuvent être délivrés par voie externe ou interne.
Essayez-le
- Comment peut-on utiliser un nucléide radioactif pour montrer que l’équilibre :\text{AgCl}\left(s\right)\rightleftharpoons {\text{Ag}}^{\text{+}}\left(aq\right)+{\text{Cl}}^{\text{-}}\left(aq\right)} est un équilibre dynamique ?
- Le technétium 99m a une demi-vie de 6,01 heures. Si un patient auquel on a injecté du technétium-99m peut quitter l’hôpital en toute sécurité une fois que 75 % de la dose s’est désintégrée, quand le patient peut-il quitter l’hôpital ?
- L’iode qui pénètre dans l’organisme est stocké dans la glande thyroïde d’où il est libéré pour contrôler la croissance et le métabolisme. La thyroïde peut être imagée si de l’iode 131 est injecté dans le corps. À plus fortes doses, l’I-133 est également utilisé pour traiter le cancer de la thyroïde. L’iode 131 a une demi-vie de 8,70 jours et se désintègre par émission β-.
- Écrire une équation pour la désintégration.
- Combien de temps faudra-t-il pour que 95.0% d’une dose d’I-131 à se désintégrer ?
Glossaire
Chémothérapie : similaire à la radiothérapie interne, mais des substances chimiques plutôt que radioactives sont introduites dans le corps pour tuer les cellules cancéreuses
Radiothérapie par faisceau externe : rayonnement délivré par une machine à l’extérieur du corps
Radiothérapie interne : (également, curiethérapie) rayonnement d’une substance radioactive introduite dans l’organisme pour tuer les cellules cancéreuses
radiothérapie : utilisation de rayonnements à haute énergie pour endommager l’ADN des cellules cancéreuses, ce qui les tue ou les empêche de se diviser
traceur radioactif : (également, étiquette radioactive) radio-isotope utilisé pour suivre ou repérer une substance en surveillant ses émissions radioactives
.